题目内容
某兴趣小组同学为了探究干电池中物质的成分,将电池剥开时闻到异味且发现有黑色物质.
【提出问题】为什么有异味?黑色物质的成分是什么?
【网络搜索】干电池的成分有二氧化锰、铁粉及铵盐等物质.
【实验探究】同学们分别设计实验进行探究.
实验Ⅰ.小婧取适量黑色物质与 混合置于研钵内研磨,嗅到氨味,再用湿润的红色石蕊试纸检测,试纸变蓝,证明黑色物质中含有铵盐.
实验Ⅱ.小清用一种物理方法发现黑色物质中不含铁粉,他采用的方法是 ;
实验Ⅲ.小明将黑色物质加入适量的水中搅拌,静置后过滤,取滤渣进行实验.
据此小明认为黑色物质中一定含有二氧化锰.
【交流讨论】大家对小明的结论提出了质疑.
(1)小莹认为若要证明黑色物质中一定含有二氧化锰,必须验证二氧化锰的质量和 在反应前后都没有发生变化;
(2)小仪认为除了小莹考虑的因素外,另一个原因是氧化铜等黑色物质对过氧化氢分解也有催化作用.
【结论反思】
(1)干电池中一定含有铵盐,可能含有二氧化锰,一定不含有铁粉.
(2)面对网络信息,我们要去伪存真.下列网络信息,说法不正确的是 .
A.用大米制作的南昌特色小吃-“南昌炒粉”,可为人体提供的主要营养素是糖类
B.某公司找到了“只用水就能变成汽油”的方法,解决了能源危机
C.涂抹呈碱性的肥皂水可减轻蚊虫叮咬分泌的蚁酸造成的皮肤痛痒.
【提出问题】为什么有异味?黑色物质的成分是什么?
【网络搜索】干电池的成分有二氧化锰、铁粉及铵盐等物质.
【实验探究】同学们分别设计实验进行探究.
实验Ⅰ.小婧取适量黑色物质与
实验Ⅱ.小清用一种物理方法发现黑色物质中不含铁粉,他采用的方法是
实验Ⅲ.小明将黑色物质加入适量的水中搅拌,静置后过滤,取滤渣进行实验.
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量黑色滤渣装入试管中,再加入过氧化氢溶液 | | 有气体生成 |
| 向上述试管中伸入带火星的小木条 | 木条复燃 | 该气体是 |
【交流讨论】大家对小明的结论提出了质疑.
(1)小莹认为若要证明黑色物质中一定含有二氧化锰,必须验证二氧化锰的质量和
(2)小仪认为除了小莹考虑的因素外,另一个原因是氧化铜等黑色物质对过氧化氢分解也有催化作用.
【结论反思】
(1)干电池中一定含有铵盐,可能含有二氧化锰,一定不含有铁粉.
(2)面对网络信息,我们要去伪存真.下列网络信息,说法不正确的是
A.用大米制作的南昌特色小吃-“南昌炒粉”,可为人体提供的主要营养素是糖类
B.某公司找到了“只用水就能变成汽油”的方法,解决了能源危机
C.涂抹呈碱性的肥皂水可减轻蚊虫叮咬分泌的蚁酸造成的皮肤痛痒.
考点:实验探究物质的组成成分以及含量,证明铵盐,氧气的检验和验满,催化剂的特点与催化作用,金属的化学性质,质量守恒定律及其应用
专题:科学探究
分析:实验Ⅰ.根据铵盐与碱混合会放出氨气进行解答;
实验Ⅱ.根据铁能被磁铁吸引进行解答;
实验Ⅲ.根据二氧化锰和过氧化氢溶液混合会生成氧气,氧气具有助燃性,能使带火星的木条复燃进行解答;
【交流讨论】(1)根据二氧化锰能加快过氧化氢溶液分解生成氧气的速率,而本身的质量和化学性质不变进行解答.
【结论反思】
A、根据常见的食品中含有的营养素进行分析,米中含有较多的淀粉,淀粉属于糖类;
B、根据质量守恒定律进行分析;
C、考虑中和反应的运用.
实验Ⅱ.根据铁能被磁铁吸引进行解答;
实验Ⅲ.根据二氧化锰和过氧化氢溶液混合会生成氧气,氧气具有助燃性,能使带火星的木条复燃进行解答;
【交流讨论】(1)根据二氧化锰能加快过氧化氢溶液分解生成氧气的速率,而本身的质量和化学性质不变进行解答.
【结论反思】
A、根据常见的食品中含有的营养素进行分析,米中含有较多的淀粉,淀粉属于糖类;
B、根据质量守恒定律进行分析;
C、考虑中和反应的运用.
解答:解:
实验Ⅰ.铵盐与碱混合会放出氨气,所以取适量黑色物质与熟石灰混合置于研钵内研磨,嗅到氨味,再用湿润的石蕊试纸检测,试纸变蓝,证明黑色物质中含有铵盐;
实验Ⅱ.铁能被磁铁吸引,所以用一种物理方法发现黑色物质中不含铁扮.他采用的方法是用磁铁吸引;
实验Ⅲ.二氧化锰和过氧化氢溶液混合会生成氧气,氧气具有助燃性,能使带火星的木条复燃,所以实验方案为:
;二氧化锰和过氧化氢溶液混合会生成氧气,化学方程式为2H2O2
2H2O+O2↑;
【交流讨论】(1)二氧化锰能加快过氧化氢溶液分解生成氧气的速率,而本身的质量和化学性质不变,所以若要证明黑色物质中一定含有二氧化锰,必须验证二氧化锰的质量和化学性质.
【结论反思】
A、大米为人体提供的营养素主要糖类;说法正确;
B、根据质量守恒定律可知:“只用水就能变成汽油”的说法错误,因为水的组成元素为氢、氧元素,不含有碳元素,故不能变成汽油,故说法错误;
C、根据中和反应可知:涂抹呈碱性的肥皂水可减轻蚊虫叮咬分泌的蚁酸造成的皮肤痛痒,说法正确;
故选:B.
故答案为:
实验Ⅰ.熟石灰;
实验Ⅱ.用磁铁吸引;
实验Ⅲ.
【交流讨论】(1)化学性质.
【结论反思】B.
实验Ⅰ.铵盐与碱混合会放出氨气,所以取适量黑色物质与熟石灰混合置于研钵内研磨,嗅到氨味,再用湿润的石蕊试纸检测,试纸变蓝,证明黑色物质中含有铵盐;
实验Ⅱ.铁能被磁铁吸引,所以用一种物理方法发现黑色物质中不含铁扮.他采用的方法是用磁铁吸引;
实验Ⅲ.二氧化锰和过氧化氢溶液混合会生成氧气,氧气具有助燃性,能使带火星的木条复燃,所以实验方案为:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取适量黑色滤渣装入试管中,再加入过氧化氢溶液 | 产生大量气泡 | 有气体生成 |
| ②立即向试管中带火星的木条 | 木条复燃 | 该气体是氧气 |
| ||
【交流讨论】(1)二氧化锰能加快过氧化氢溶液分解生成氧气的速率,而本身的质量和化学性质不变,所以若要证明黑色物质中一定含有二氧化锰,必须验证二氧化锰的质量和化学性质.
【结论反思】
A、大米为人体提供的营养素主要糖类;说法正确;
B、根据质量守恒定律可知:“只用水就能变成汽油”的说法错误,因为水的组成元素为氢、氧元素,不含有碳元素,故不能变成汽油,故说法错误;
C、根据中和反应可知:涂抹呈碱性的肥皂水可减轻蚊虫叮咬分泌的蚁酸造成的皮肤痛痒,说法正确;
故选:B.
故答案为:
实验Ⅰ.熟石灰;
实验Ⅱ.用磁铁吸引;
实验Ⅲ.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取适量黑色滤渣装入试管中,再加入过氧化氢溶液 | 产生大量气泡 | 有气体生成 |
| ②立即向试管中带火星的木条 | 木条复燃 | 该气体是氧气 |
【结论反思】B.
点评:本题是一个综合性很强的实验题,难度较大.试题涉及到了试验设计、常见离子组的鉴别.学生对方程式的书写应熟练掌握.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
下列有关金属性质的说法错误的是( )
| A、埋在潮湿、疏松、透气的酸性土壤中的铸铁管容易被腐蚀 |
| B、在空气中灼烧铜丝,其表面会变黑 |
| C、铜、银等金属具有良好的导电性 |
| D、常温下所有金属是银白色固体 |

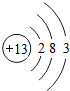 ,铝原子在化学反应中容易
,铝原子在化学反应中容易