题目内容
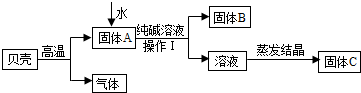
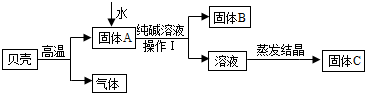
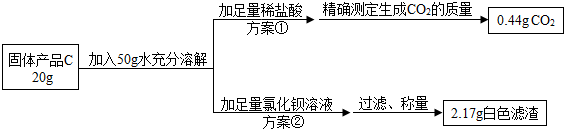
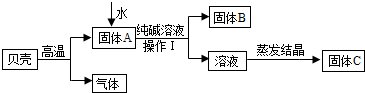
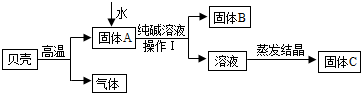
在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱,某小组同学按图所示流程进行实验,请你参与讨论并回答相关问题.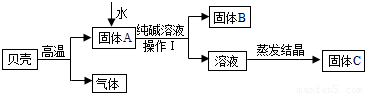
(1)贝壳高温煅烧时,发生反应的化学方程式是 ;
(2)水加入到固体A中形成的是 (填溶液、乳浊液或悬浊液).操作Ⅰ中用到的玻璃仪器有烧杯、 、玻璃棒;
(3)在上述整个过程中没有涉及到的化学反应类型是 反应.
(4)将固体C配成溶液,其溶液中一定含有的溶质是 .
【答案】分析:(1)根据碳酸钙分解的反应原理书写方程式;
(2)根据固体A是否可溶进行判断,依据过滤的特点与过滤所用仪器分析解答;
(3)得把每部反应进行推理,然后对反应类型进行判断;
(4)判断溶质先看反应的生成物,再看反应物手否有剩余.
解答:解:(1)碳酸钙高温分解生成氧化钙和二氧化碳,方程式是:CaCO3 CaO+CO2↑;
CaO+CO2↑;
故答案为:CaCO3 CaO+CO2↑;
CaO+CO2↑;
(2)固体A为氧化钙,溶于水生成熟石灰,由于熟石灰微溶于水,所以形成的为悬浊液;操作Ⅰ是将不溶水的固体物质与液体分离,符合过滤的特点,故此操为过滤,过滤用到的玻璃仪器有:烧杯、漏斗、玻璃棒;
故答案为:悬浊液,漏斗;
(3)贝壳高温分解为氧化钙和二氧化碳,属于分解反应;氧化钙与水反应生成氢氧化钙,属于化合反应;氢氧化钙溶液与纯碱溶液反应生成碳酸钙沉淀和氢氧化钠,属于复分解反应;故缺少置换反应;
故答案为:置换反应
(4)氢氧化钙溶液与纯碱溶液反应生成碳酸钙沉淀和氢氧化钠,碳酸钙为沉淀不能做溶质,只能是氢氧化钠做溶质;而反应物不知是否过量,所以氢氧化钙或碳酸钠只能是可能存在;
故答案为:NaOH.
点评:本题是一道结合实验流程图探究烧碱制备的实验探究题,考查了学生依据相关知识分析、解决问题的能力;分析问题时要考虑全面,才能正确解答.
(2)根据固体A是否可溶进行判断,依据过滤的特点与过滤所用仪器分析解答;
(3)得把每部反应进行推理,然后对反应类型进行判断;
(4)判断溶质先看反应的生成物,再看反应物手否有剩余.
解答:解:(1)碳酸钙高温分解生成氧化钙和二氧化碳,方程式是:CaCO3
 CaO+CO2↑;
CaO+CO2↑;故答案为:CaCO3
 CaO+CO2↑;
CaO+CO2↑;(2)固体A为氧化钙,溶于水生成熟石灰,由于熟石灰微溶于水,所以形成的为悬浊液;操作Ⅰ是将不溶水的固体物质与液体分离,符合过滤的特点,故此操为过滤,过滤用到的玻璃仪器有:烧杯、漏斗、玻璃棒;
故答案为:悬浊液,漏斗;
(3)贝壳高温分解为氧化钙和二氧化碳,属于分解反应;氧化钙与水反应生成氢氧化钙,属于化合反应;氢氧化钙溶液与纯碱溶液反应生成碳酸钙沉淀和氢氧化钠,属于复分解反应;故缺少置换反应;
故答案为:置换反应
(4)氢氧化钙溶液与纯碱溶液反应生成碳酸钙沉淀和氢氧化钠,碳酸钙为沉淀不能做溶质,只能是氢氧化钠做溶质;而反应物不知是否过量,所以氢氧化钙或碳酸钠只能是可能存在;
故答案为:NaOH.
点评:本题是一道结合实验流程图探究烧碱制备的实验探究题,考查了学生依据相关知识分析、解决问题的能力;分析问题时要考虑全面,才能正确解答.

练习册系列答案
相关题目