题目内容
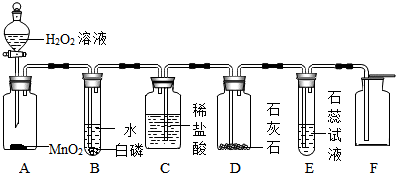
某同学利用“多米诺骨牌”效应,设计了如图气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色,请看图回答问题:
(1)B中白磷不燃烧,原因是 ;
(2)D中发生反应的化学方程式为: ;
(3)用化学方程式表示E种颜色变化的原因 ;用F装置收集气体的依据是 .

(1)B中白磷不燃烧,原因是
(2)D中发生反应的化学方程式为:
(3)用化学方程式表示E种颜色变化的原因
考点:实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式,燃烧与燃烧的条件
专题:综合实验题
分析:(1)根据燃烧的条件分析:与氧气接触、温度达到着火点;
(2)盐酸在氧气的作用下被压进D中,与石灰石反应;
(3)根据二氧化碳与水反应生成碳酸能使石蕊试液变成红色分析;二氧化碳的密度比空气大,采用向上排空气法收集;
(2)盐酸在氧气的作用下被压进D中,与石灰石反应;
(3)根据二氧化碳与水反应生成碳酸能使石蕊试液变成红色分析;二氧化碳的密度比空气大,采用向上排空气法收集;
解答:解:
(1)B中白磷不燃烧,由于左侧产生氧气进入了B装置,所以应该是温度没有达到着火点.原因是:温度没有达到着火点.
(2)氧气不与盐酸反应,所以氧气把盐酸从C装置压人D装置,与石灰石反应,产生气泡,反应的方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)多余的二氧化碳进入E装置与水反应产生碳酸,使紫色的石蕊试液变成红色;反应的方程式为:CO2+H2O═H2CO3;因为二氧化碳的密度比空气大,所以可以采用向上排空气法收集;
答案:
(1)温度没有达到着火点
(2)产生气泡 CaCO3+2HCl═CaCl2+H2O+CO2↑
(3)CO2+H2O═H2CO3
二氧化碳的密度比空气大
(1)B中白磷不燃烧,由于左侧产生氧气进入了B装置,所以应该是温度没有达到着火点.原因是:温度没有达到着火点.
(2)氧气不与盐酸反应,所以氧气把盐酸从C装置压人D装置,与石灰石反应,产生气泡,反应的方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)多余的二氧化碳进入E装置与水反应产生碳酸,使紫色的石蕊试液变成红色;反应的方程式为:CO2+H2O═H2CO3;因为二氧化碳的密度比空气大,所以可以采用向上排空气法收集;
答案:
(1)温度没有达到着火点
(2)产生气泡 CaCO3+2HCl═CaCl2+H2O+CO2↑
(3)CO2+H2O═H2CO3
二氧化碳的密度比空气大
点评:掌握氧气的反应原理、二氧化碳的实验室制法及其物理性质和化学性质;了解燃烧与燃烧的条件,并能结合题目装置分析解答.

练习册系列答案
相关题目
 如图是用比例模型来表示物质间发生化学变化的微观示意图.图中“
如图是用比例模型来表示物质间发生化学变化的微观示意图.图中“ ”和“
”和“ ”分别表示两种元素的原子,能用该图示表示的化学反应是( )
”分别表示两种元素的原子,能用该图示表示的化学反应是( )A、2H2+O2
| ||||
| B、CO2+H2O═H2CO3 | ||||
C、2CO+O2
| ||||
D、H2+Cl2
|