题目内容
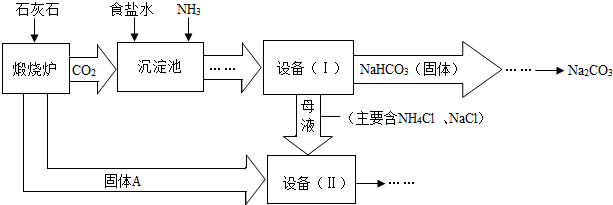
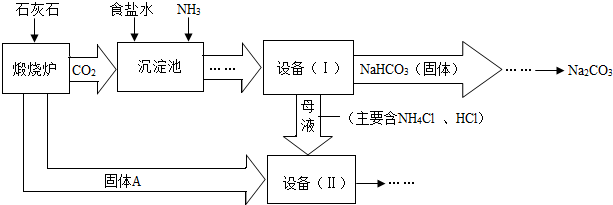
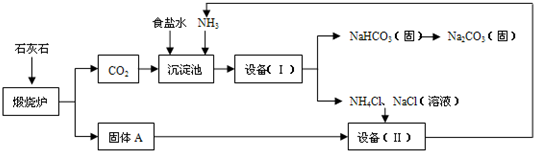
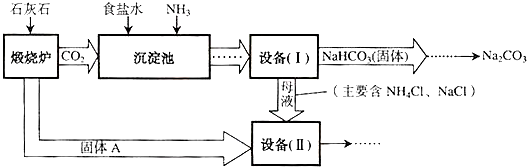
工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让NaCl、NH3、CO2和H2O尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液).主要生产流程如下:(已知2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O)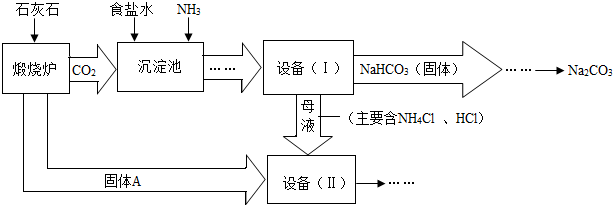
(1)“煅烧炉”中发生反应的化学方程式是______.
(2)若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是______,该操作中用到的玻璃仪器有烧杯、______和______.
(3)在“设备(Ⅱ)”中固体A与水反应的化学方程式是______.
(4)对“设备(Ⅱ)”中的母液处理后,除水以外可在本流程中再利用的物质有______(填写化学式).
(5)请写出纯碱(Na2CO3)的一点用途:______.
解:(1)碳酸钙在高温下分解生成二氧化碳气体和氧化钙,方程式为:CaCO3 CaO+CO2↑;
CaO+CO2↑;
(2)过滤是把不溶于液体的固体和液体分开的一种分离混合物的方法,“设备(I)”中的液体混合物中分离出析出的晶体,故可用过滤的方法;过滤用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(3)氧化钙与水反应生成氢氧化钙,方程式为:H2O+CaO=Ca(OH)2;
(4)进入“设备(Ⅱ)”的物质有氧化钙、氯化钠、氯化铵及水,发生的反应有H2O+CaO=Ca(OH)2、Ca(OH)2+2NH4Cl=2NH3↑+2H2O+CaCl2,最终产物有氯化钠、氯化钙、氨气,其中氯化钠、氨气可再利用;
(5)纯碱是一种重要的关于用品,可用于玻璃、造纸、纺织或洗涤剂的生产等;
故答案为:
(1)CaCO3 CaO+CO2↑;
CaO+CO2↑;
(2)过滤;漏斗、玻璃棒;
(3)H2O+CaO=Ca(OH)2;
(4)NH3、NaCl;
(5)用于玻璃、造纸、纺织或洗涤剂的生产等.
分析:(1)根据碳酸钙高温分解的化学性质回答;
(2)根据过滤的原理和适用范围、以及所用的仪器回答;
(3)根据氧化钙的化学性质书写方程式;
(4)根据“设备(Ⅱ)”中发生的反应和流程图中可循环使用的物质回答;
(5)根据纯碱的用途回答.
点评:本题看起来起点很高,但落点较低,考查了学生对知识的理解和应用,也充分体现了化学来源于生产、生活,又服务于生产、生活的理念.
 CaO+CO2↑;
CaO+CO2↑;(2)过滤是把不溶于液体的固体和液体分开的一种分离混合物的方法,“设备(I)”中的液体混合物中分离出析出的晶体,故可用过滤的方法;过滤用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(3)氧化钙与水反应生成氢氧化钙,方程式为:H2O+CaO=Ca(OH)2;
(4)进入“设备(Ⅱ)”的物质有氧化钙、氯化钠、氯化铵及水,发生的反应有H2O+CaO=Ca(OH)2、Ca(OH)2+2NH4Cl=2NH3↑+2H2O+CaCl2,最终产物有氯化钠、氯化钙、氨气,其中氯化钠、氨气可再利用;
(5)纯碱是一种重要的关于用品,可用于玻璃、造纸、纺织或洗涤剂的生产等;
故答案为:
(1)CaCO3
 CaO+CO2↑;
CaO+CO2↑;(2)过滤;漏斗、玻璃棒;
(3)H2O+CaO=Ca(OH)2;
(4)NH3、NaCl;
(5)用于玻璃、造纸、纺织或洗涤剂的生产等.
分析:(1)根据碳酸钙高温分解的化学性质回答;
(2)根据过滤的原理和适用范围、以及所用的仪器回答;
(3)根据氧化钙的化学性质书写方程式;
(4)根据“设备(Ⅱ)”中发生的反应和流程图中可循环使用的物质回答;
(5)根据纯碱的用途回答.
点评:本题看起来起点很高,但落点较低,考查了学生对知识的理解和应用,也充分体现了化学来源于生产、生活,又服务于生产、生活的理念.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目