题目内容
【题目】为了测定混有少量杂质的高锰酸钾固体样品中高锰酸钾的质量分数,取20g样品加热(杂质不反应),剩余固体的质量与加热时间的关系如表所示:
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
剩余固体质量/g | 20 | 20 | 19.6 | 18.8 | 18.6 | 18.4 | 18.4 |
(1)反应中产生氧气的质量是___________g。
(2)求样品中高锰酸钾的质量分数_________。
【答案】1.6 79%
【解析】
(1)根据质量守恒定律,反应前后固体减少的质量即生成氧气的质量,反应中产生氧气的质量是20g-18.4g=1.6g。
(2)解:设样品中高锰酸钾的质量x·

![]()
x=15.8g
样品中高锰酸钾的质量分数为=![]() ·
·
答:样品中高锰酸钾的质量分数为79%·

练习册系列答案
相关题目
【题目】实验室制气体常见仪器如下图所示。
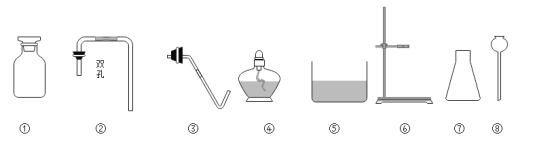
A | B |
用过氧化氢溶液与二氧化锰制氧气。 (1)反应的化学方程式为_____。 (2)组装发生装置应选择的仪器为_____(填序号)。 | 用加热高锰酸钾的方法制氧气 (1)反应的化学方程式为_____。 (2)需要补充的一种仪器是_____。 |