题目内容
16.(1)用化学符号表示:①缺Ca有可能导致骨骼疏松,②氨分子NH3,③硅原子Si,④铁离子Fe3+,⑤氧化铝中铝元素的化合价$\stackrel{+3}{Al}$2O3,⑥溶于水使温度显著降低的盐NH4NO3.
(2)写出下列反应的化学方程式:
①铁丝在氧气中燃烧3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,②二氧化碳通入澄清石灰水CO2+Ca(OH)2=CaCO3↓+H2O,
③用稀盐酸除去铁锈Fe2O3+6HCl=2FeCl3+3H2O,④在烧碱溶液中滴加硫酸铜溶液CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
分析 (1)元素符号可以表示一种元素,还可以表示该元素的1个原子,有时还可以表示一种物质,例如金属元素的元素符号可以表示该金属元素组成的物质;
每个氨气分子由1个氮原子和3个氢原子构成;
每个铁离子带3个单位正电荷;
元素的化合价应该标在元素符号正上方;
硝酸铵溶于水时吸收热量;
(2)铁在氧气中燃烧生成四氧化三铁;
二氧化碳能和石灰水中的氢氧化钙反应生成碳酸钙沉淀和水;
氧化铁和稀盐酸反应生成氯化铁和水;
硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠.
解答 解:(1)①缺Ca元素有可能导致骨骼疏松;
②氨分子可以表示为NH3;
③硅原子可以表示为Si;
④铁离子可以表示为Fe3+;
⑤氧化铝中铝元素的化合价是+3,可以表示为$\stackrel{+3}{Al}$2O3;
⑥溶于水使温度显著降低的盐是硝酸铵,可以表示为NH4NO3.
故填:Ca;NH3;Si;Fe3+;$\stackrel{+3}{Al}$2O3;NH4NO3.
(2)①铁丝在氧气中燃烧的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
②二氧化碳通入澄清石灰水时,二氧化碳和氢氧化钙反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
③用稀盐酸除去铁锈的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;
④在烧碱溶液中滴加硫酸铜溶液时,硫酸铜和氢氧化钠反应的化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
故填:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;CO2+Ca(OH)2=CaCO3↓+H2O;Fe2O3+6HCl=2FeCl3+3H2O;CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
点评 本题主要考查学生对化学用语的书写和理解能力,题目重点考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | 分别通入无色酚酞试液 | B. | 分别放入一根带火星的木条 | ||
| C. | 分别通过灼热的氧化铜 | D. | 闻气味 |
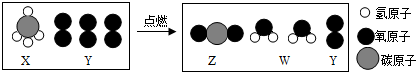
| A. | 化学反应前后原子的种类、个数、质量都不变 | |
| B. | X物质中碳元素的质量分数为75.0% | |
| C. | 该反应的化学方程式为CH4+3O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O+O2 | |
| D. | 该反应中反应物X、Y的分子个数比为1:2 |

| A. | ①②③ | B. | ①② | C. | ②④ | D. | ①②④ |
| A. | 黑芥子甙是由碳、氢、氧、氮、硫五种元素组成的 | |
| B. | 黑芥子甙中硫、氧两种元素的质量比为4:9 | |
| C. | 黑芥子甙在氧气中充分燃烧只生成CO2和H2O | |
| D. | 黑芥子甙中含量最多的元素是氧元素 |

