题目内容
9.2011年“3•15晚会”曝光河南双汇火腿“瘦肉精”事件(“瘦肉精”的化学式为C6H19OCl3N2).下列有关“瘦肉精”的说法正确的是( )| A. | “瘦肉精”分子的相对分子质量为241.5 | |
| B. | “瘦肉精”含有31个原子 | |
| C. | “瘦肉精”属于氧化物 | |
| D. | “瘦肉精”中氢元素的质量分数最大 |
分析 A.根据相对分子质量的计算方法来分析;
B.根据物质的结构来分析;
C.氧化物中含有两种元素;
D.根据化合物中元素的质量比来分析.
解答 解:A.由瘦肉精的化学式为C6H19OCl3N2可知,则相对分子质量为12×6+1×19+35.5×3+14×2+16=241.5,故正确;
B.“瘦肉精”是由分子构成的,而不是由原子直接构成的,故错误;
C.由瘦肉精的化学式为C6H19OCl3N2可知,它是由五种元素组成的,不属于氧化物,故错误;
D.“瘦肉精”中碳、氢、氧、氯、氮五种元素的质量比为(12×6):(1×19):16:(35.5×3):(14×2)=72:19:16:106.5:28,可见其中氯元素的质量分数最高,故错误.
故选A.
点评 本题考查学生利用信息种物质的化学式进行简单计算,明确化学式计算的方法即可解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列各组气体,可用同一方法收集的是( )
| A. | H2、O2、CO2 | B. | H2、O2、CO | C. | H2、CO、CO2 | D. | O2、CO2、CO |
4.甲醛(化学式为CH2O)是室内装潢时的主要污染物之一,下列关于甲醛的说法正确的是( )
| A. | 甲醛是由碳、氢、氧三种元素组成的 | |
| B. | 甲醛是由碳原子和水分子构成的 | |
| C. | 甲醛由一个碳原子、两个氢原子、一个氧原子构成 | |
| D. | 甲醛由一个碳元素、两个氢元素、一个氧元素组成的 |
1.下列对分子、原子、离子的认识,正确的是( )
| A. | 原子是最小的粒子,不可再分 | |
| B. | 氮分子是保持氮气化学性质的最小微粒 | |
| C. | 离子不能直接构成物质 | |
| D. | 固体难压缩,说明固体分子间无间隔 |
3.现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠四种无色溶液,为了确定四种溶液各是什么,将它们随意编号为A、B、C、D后,按照下表进行实验,产生的现象如下所示:
根据实验现象按要求回答:
(1)A、B、C溶液的溶质化学式:
ACaCl2;
BHCl;
CAgNO3.
(2)写出实验顺序①②③④有关的离子方程式,不反应的说明理由:
①不具备复分解反应发生的条件,
②CO32-+2H+=CO2↑+H2O,
③Cl-+Ag+=AgCl↓,
④CO32-+Ca2+=CaCO3↓.
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 没有现象 |
| ② | B+D | 有气体放出 |
| ③ | C+B | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
(1)A、B、C溶液的溶质化学式:
ACaCl2;
BHCl;
CAgNO3.
(2)写出实验顺序①②③④有关的离子方程式,不反应的说明理由:
①不具备复分解反应发生的条件,
②CO32-+2H+=CO2↑+H2O,
③Cl-+Ag+=AgCl↓,
④CO32-+Ca2+=CaCO3↓.

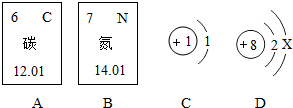 下图A、B是碳元素和氮元素在元素周期表中的部分信息,C、D是两种粒子的结构示意图.仔细观察,按要求回答下列问题:
下图A、B是碳元素和氮元素在元素周期表中的部分信息,C、D是两种粒子的结构示意图.仔细观察,按要求回答下列问题: