题目内容
19. 钢是铁的合金.为测定某钢样中铁的质量分数,取11.4g钢样,向其中加入稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如图所示(不考虑钢样中其它成分与稀硫酸的反应).
钢是铁的合金.为测定某钢样中铁的质量分数,取11.4g钢样,向其中加入稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如图所示(不考虑钢样中其它成分与稀硫酸的反应).(1)钢是(填“是”或“不是”)金属材料.
(2)计算此钢样中铁的质量分数.
分析 (1)金属材料包括纯金属材料和合金材料;
(2)根据生成的氢气的质量和对应的化学方程式求算铁的质量,进而求算其质量分数.
解答 解:
(1)钢属于铁的合金,属于金属材料;
(2)设参加反应的铁的质量为x
Fe+H2SO4=FeSO4+H2↑
56 2
x 0.4g
$\frac{56}{2}$=$\frac{x}{0.4g}$
x=11.2g
此钢样中铁的质量分数为$\frac{11.2g}{11.4g}$×100%≈98.2%
答:(1)钢是金属材料.
(2)此钢样中铁的质量分数约为98.2%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
7.下列做法合理的是( )
| A. | 用小苏打除去面团发酵产生的酸 | B. | 用白醋长时间浸泡铝壶内的水垢 | ||
| C. | 用食盐除去铁锅内的油污 | D. | 用燃着的火柴检查煤气罐是否漏气 |
14.下列做法不正确的是( )
| A. | 为使农作物增产,大量施用化肥和农药 | |
| B. | 食用水果、蔬菜水果补充维生素 | |
| C. | 重复使用某些塑料制品,减少“白色污染” | |
| D. | 炒菜时油锅着火,用锅盖盖灭 |
11.如图表示某化学反应的微观示意图,依据图分析判断,下列说法正确的是( )
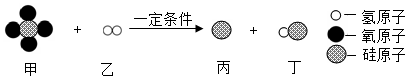

| A. | 甲物质由5个原子构成 | |
| B. | 化学变化前后硅元素的化合价不变 | |
| C. | 参加反应的乙的质量和生成的丁中氢元素的质量相等 | |
| D. | 参加反应的甲、乙两种物质的分子个数比为1:1 |
8.如图为两种物质间发生化学反应的微观示意图(一种小球代表一种原子).下列说法中正确的是( )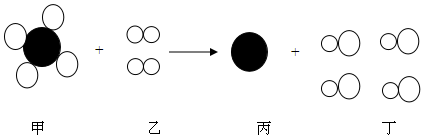

| A. | 该反应属于复分解反应 | B. | 1个甲分子由5个原子组成 | ||
| C. | 该示意图中共有2种化合物分子 | D. | 反应中乙、丁两物质的质量比为1:2 |
 如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.
如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.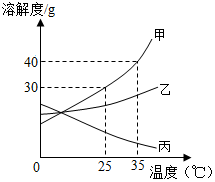 甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题: