题目内容
有人设计如下图所示的装置来验证质量守恒定律:把装有硫酸铜溶液的小试管放人盛有氢氧化钠溶液的烧杯中,将烧杯放到托盘天平上,用砝码平衡。取下烧杯并将其倾斜,使两种溶液混合反应,再把烧杯放到天平上,观察天平是否平衡。你认为上述实验设计是否严密?请说明理由。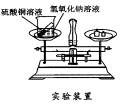
答案:
解析:
提示:
解析:
| 不严密。因为氢氧化钠溶液可跟空气中的二氧化碳反应。
|
提示:

练习册系列答案
相关题目