题目内容
6.图中的物质为初中化学所学的物质,其中Y是铁锈的主要成分,F是一种常见的建筑材料,K可用于制洗涤剂的盐,J、H是黑色粉末.图中“-”表示两端的物质间能发生反应;“→”表示物质间存在转化关系;部分反应物或生成物已略去.
(1)写出A可能的化学式CH4;B的化学式H2O;N的一种俗名烧碱、火碱或苛性钠
(2)B+D的反应能放热(填“吸热”或“放热”)
(3)写出下列反应方程式
①G+Y的反应3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2②C+F的反应CO2+Ca(OH)2=CaCO3↓+H2O③K+F的反应Ca(OH)2+Na2CO3=2NaOH+CaCO3↓.
分析 Y是铁锈的主要成分,因此Y是氧化铁;Y能够和E既G反应,且B能够通电产生E,因此B是水,E是还原性的氢气,A燃烧产生水和C,C和黑色J反应产生G,G也能和氧化铁反应,因此C是二氧化碳,J是碳,则G是一氧化碳,反应产生H是黑色的铁;B和D反应产生F,F能够和K反应,F是一种常见的建筑材料,K可用于制洗涤剂的盐,因此F是氢氧化钙,K是碳酸钠,则D是氧化钙;氢氧化钙和碳酸钠反应产生碳酸钙沉淀和氢氧化钠,二氧化碳和氢氧化钙反应也产生M,因此M是碳酸钙,N是氢氧化钠,带入验证完成相关的问题.
解答 解:Y是铁锈的主要成分,因此Y是氧化铁;Y能够和E既G反应,且B能够通电产生E,因此B是水,E是还原性的氢气,A燃烧产生水和C,C和黑色J反应产生G,G也能和氧化铁反应,因此C是二氧化碳,J是碳,则G是一氧化碳,反应产生H是黑色的铁;B和D反应产生F,F能够和K反应,F是一种常见的建筑材料,K可用于制洗涤剂的盐,因此F是氢氧化钙,K是碳酸钠,则D是氧化钙;氢氧化钙和碳酸钠反应产生碳酸钙沉淀和氢氧化钠,二氧化碳和氢氧化钙反应也产生M,因此M是碳酸钙,N是氢氧化钠,带入验证符合转化关系,因此:
(1)A可以是甲烷,B是水,N是氢氧化钠,俗名烧碱、火碱或苛性钠;故填:CH4;H2O;烧碱、火碱或苛性钠;
(2)氧化钙溶于水,能放出热量;故填:放热;
(3)①G+Y的反应是一氧化碳和氧化铁反应产生铁和二氧化碳;②C+F的反应是二氧化碳和氢氧化钙反应产生碳酸钙沉淀和水;③K+F的反应是氢氧化钙和碳酸钠反应产生碳酸钙沉淀和氢氧化钠;故方程式分别为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;CO2+Ca(OH)2=CaCO3↓+H2O;Ca(OH)2+Na2CO3=2NaOH+CaCO3↓.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证,只要合理即可.

| A. | 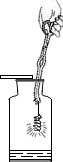 铁丝在氧气中燃烧 | B. | 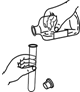 倾倒液体 | ||
| C. | 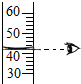 读取液体的体积 | D. | 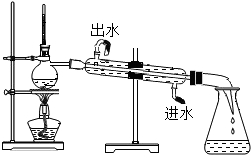 制取蒸馏水 |
| A. | 金刚石、石墨和C60里,碳原子排列方式不同 | |
| B. | 碳、一氧化碳、二氧化碳,都具有还原性 | |
| C. | 在炉子上放一盆水,就能防止一氧化碳中毒 | |
| D. | 一氧化碳和二氧化碳组成元素相同,所以化学性质相似 |
| A有关判断 | B能源与资源 |
| 水和冰的共存物----是纯净物也是氧化物 木材燃烧质量减小----符合质量守恒定律 | 天然气、可燃冰----主要成分都是CH4,是较清洁的燃料 焦炉煤气----煤干馏的产物,燃烧不会产生二氧化碳 |
| C燃烧与灭火 | D化学与生活 |
| 白磷易自然而红磷不易----着火点不同 吹灭蜡烛----降低蜡烛着火点 | 食醋----铁锅做饭时,加食醋可为人体补铁 钢----只含金属元素 |
| A. | A | B. | B | C. | C | D. | D |



 右图是细铁丝在氧气中燃烧的实验,根据图片回答下列问题.
右图是细铁丝在氧气中燃烧的实验,根据图片回答下列问题.