题目内容
11.为了测定某石灰石样品中碳酸钙的含量,取该石灰石样品粉末25g投入到200g的稀盐酸中(杂质不溶于水也不参加反应),碳酸钙全部反应后,过滤,得溶液质量为211.2g,则此石灰石样品中碳酸钙的含量为( )| A. | 80% | B. | 44.8% | C. | 55.2% | D. | 20% |
分析 根据质量守恒定律可知,碳酸钙与盐酸反应后生成氯化钙、水和二氧化碳,溶液的质量增加为常见反应的碳酸钙质量-二氧化碳质量进行分析.
解答 解:设石灰石样品中碳酸钙质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O 溶液质量增加为
100 44 100-44=56
x 211.2g-200g=11.2g
$\frac{100}{x}=\frac{56}{11.2g}$
x=20g
此石灰石样品中碳酸钙的含量为$\frac{20g}{25g}×100%$=80%.
故选:A.
点评 本题主要考查化学方程式的书写和有关化学方程式的计算,难度较大.注意:根据化学方程式计算的方法、格式和步骤.

练习册系列答案
相关题目
1.下列现象不能用质量守恒定律解释的是( )
| A. | 蜡烛燃烧时慢慢变短 | B. | 澄清石灰水露置在空气中变重 | ||
| C. | 镁带燃烧时,生成物的质量会增加 | D. | 100g干冰完全汽化成100g气体 |
19.生活及生产中的下列做法错误的是( )
| A. | 为了保护树木,用含有硫磺粉等的石灰浆粉刷树干 | |
| B. | 为了延长食品保质期,用食盐来腌渍蔬菜、鱼、肉、蛋等 | |
| C. | 为了治疗胃酸过多症,服用适量的小苏打 | |
| D. | 为了建筑物美观,用石灰石做内墙的墙面材料 |
6.在实验室,若不慎把氢氧化钠沾到皮肤上,可以用硼酸溶液处理,硼酸(化学式:H2BO3),为白色粉末状结晶或三斜轴面鳞片状光泽结晶,有滑腻手感,无臭味,溶于水、酒精、甘油、醚类及香精油中,水溶液呈弱酸性.下列关于硼酸的说法正确的是( )
| A. | 硼酸属于化合物中的氧化物 | |
| B. | 硼酸分子中氢元素、硼元素、氧元素的质量比为3:11:48 | |
| C. | 硼酸分子由3个氢原子、1个硼原子和3个氧原子构成 | |
| D. | 硼酸溶液可以与氢氧化钠反应 |
3.对于具有相同质子数的粒子,下列叙述正确的是( )
| A. | 一定是同种元素 | B. | 一定是由同种元素组成的粒子 | ||
| C. | 一定具有相同的电子数 | D. | 可能是单质,也可能是化合物 |
20.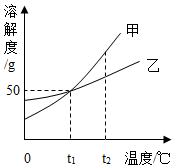 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述正确的是( )
如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述正确的是( )
 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述正确的是( )
如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述正确的是( )| A. | t1℃时,甲、乙两种物质的溶解度均为50 | |
| B. | t2℃时,甲、乙两种饱和溶液中含有甲的质量一定大于乙 | |
| C. | 甲中含有少量乙时,一般用冷却热饱和溶液的方法提纯乙 | |
| D. | t1℃时,向300g甲物质的饱和溶液中加水,可以稀释成500g质量分数20%的甲溶液 |
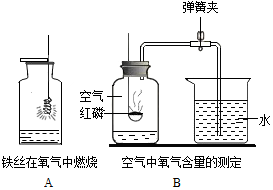 下列是初中化学常见的两个实验,回答下列问题:
下列是初中化学常见的两个实验,回答下列问题: