题目内容
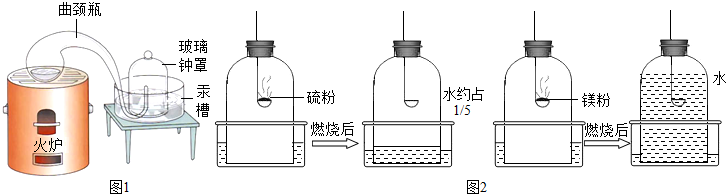
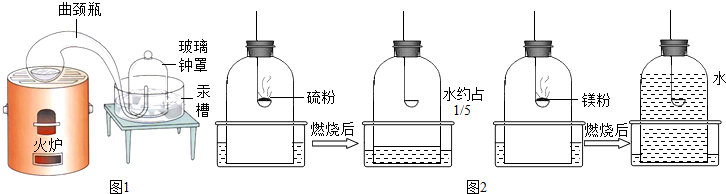
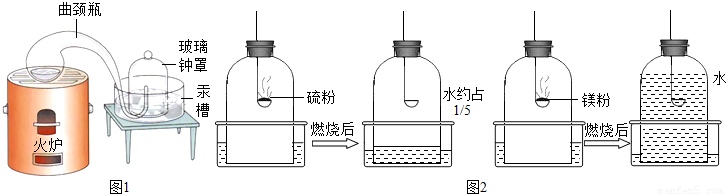
十八世纪法国化学家拉瓦锡为了研究空气的组成设计 了一个划时代意义的钟罩实验(如右图),该实验证明了空气中氧气约占空气的体积1/5。
①拉瓦锡在观察到汞面浮起红色渣滓后,还继续加热12天,至红色渣滓不再增加,这样做的理由是 (1) ,该反应的化学方程式是(2) 。
②拉瓦锡得到的红色渣滓是氧化汞,他又将氧化汞加热分解得到氧气,而现在实验室检验氧气的方法可以是(3) 。
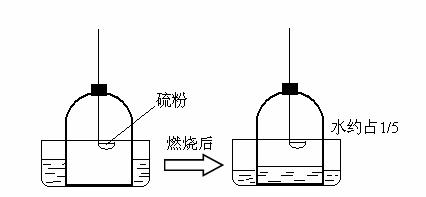 ③实验室常用白磷燃烧来验证空气中氧气约占1/5,小张同学利用实验室现有的药品硫粉和镁粉,利用下列钟罩装置进行实验,燃烧完毕冷却后的结果如图:
③实验室常用白磷燃烧来验证空气中氧气约占1/5,小张同学利用实验室现有的药品硫粉和镁粉,利用下列钟罩装置进行实验,燃烧完毕冷却后的结果如图:
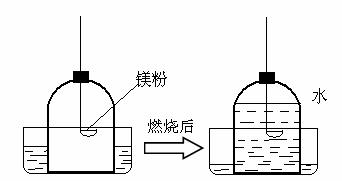
写出硫粉在钟罩内燃烧的化学方程式(4) ,燃烧的现象是(5) 。
如果实验仪器气密性良好,所用的硫粉、镁粉都是足量的。根据实验结果,推测可能的原因,硫粉燃烧后水进入约1/5的原因是(6) ;镁粉燃烧后水几乎占满整个钟罩的原因是(7) 。
④现在实验室中得到氧气,可以利用氯酸钾受热分解,实验操作时要用到酒精灯、导管、铁架台等,还需用到的玻璃仪器有(8) ;目前实验室不用氧化汞加热分解的方法制取氧气的理由是(9) 。
⑤若实验室利用12.25g氯酸钾与3gMnO2混合加热,请写出化学反应方程式,并列式计算最多可以得到多少物质的量的氧气?
(1)确保O2 完全被消耗
 (2)2Hg+ O2 △ 2HgO
(2)2Hg+ O2 △ 2HgO
(3)用带火星的木条检验,若木条复燃,则是O2
(4) (5)产生微弱的淡蓝色火焰
(5)产生微弱的淡蓝色火焰
(6) 燃烧消耗
燃烧消耗 ,生成
,生成 溶于水,钟罩内气压减小
溶于水,钟罩内气压减小
(7) 与空气中多种成分反应(
与空气中多种成分反应( 、
、 、
、 )
)
(8)试管、集气瓶、水槽
(9)汞有毒;反应时间过长,不利于操作
(10)解:设最多可得到




 解得:
解得:
答:最多可以得到 的氧气。
的氧气。

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案