题目内容
12.3月22日式世界节水日,2013年“世界水日”的宣传主题是“水合作”.我国纪念2013年“世界水日”和“中国水周”活动的宣传主题为“节约保护水资源,大力建设生态文明”.(1)云南连续几年干旱,严重缺水.
①有些村民打井取用地下水,可用检验地下水是硬水还是软水,生活中可以利用煮沸的方法降低水的硬度;
②有些村民取用浑浊的河水,加入明矾处理后作为生活用水.明矾可用于净水,是因为明矾溶于水生成胶状物质可以悬浮于水中的杂质,使之从水中沉降出来;
③天干物燥,容易引发火灾.消防员高压水枪灭火的原理是降低可燃物的温度到着火点以下.
(2)甲、乙、丙三种物质的溶解度曲线如图所示.据图回答:

①50℃时,乙物质的溶解度是40g;
②30℃时,三种物质的溶解度由大到小的顺序为乙、甲、丙;
③要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是:升高温度;
④50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是甲,所得溶液中溶质质量分数最小的是丙.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)①生活中可以利用煮沸的方法降低水的硬度;
③消防员高压水枪灭火的原理是:降低可燃物的温度到着火点以下;
(2)①通过分析溶解度曲线可知,50℃时,乙物质的溶解度是40g;
②30℃时,三种物质的溶解度由大到小的顺序为乙、甲、丙;
③丙物质的溶解度随温度的升高而减小,所以要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是:升高温度;
④甲物质的溶解度受温度影响变化最大,丙物质降低温度不会析出晶体,丙物质50℃时的溶解度小于甲、乙物质10℃时的溶解度,所以50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是甲,所得溶液中溶质质量分数最小的丙.
故答案为:(1)①煮沸;
③降低可燃物的温度到着火点以下;
(2)①40;
②乙、甲、丙;
③升高温度;
④甲,丙.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
2.某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验.
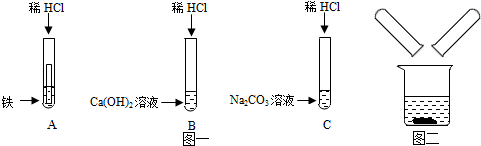
(1)A试管中的反应现象是铁片表面有气泡产生,溶液由无色逐渐变为浅绿色.
(2)C试管中反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
【提出猜想】
甲同学猜想:有NaCl
乙同学猜想:有NaCl、CaCl2
丙同学猜想:有NaCl、CaCl2、HCl
你的猜想:有NaCl、Na2CO3.
【交流讨论】
你认为丙同学的猜想一定不正确,理由是Na2CO3先和HCl反应,当HCl过量时,Na2CO3被完全反应,不可能再与CaCl2反应生成白色沉淀.
【设计实验】请设计实验证明你的猜想正确.
【反思与总结】判断反应后溶液中溶质的成分,除要考虑生成物外,还需考虑反应物是否有剩余(表述合理即可)..

(1)A试管中的反应现象是铁片表面有气泡产生,溶液由无色逐渐变为浅绿色.
(2)C试管中反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
【提出猜想】
甲同学猜想:有NaCl
乙同学猜想:有NaCl、CaCl2
丙同学猜想:有NaCl、CaCl2、HCl
你的猜想:有NaCl、Na2CO3.
【交流讨论】
你认为丙同学的猜想一定不正确,理由是Na2CO3先和HCl反应,当HCl过量时,Na2CO3被完全反应,不可能再与CaCl2反应生成白色沉淀.
【设计实验】请设计实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向其中滴加无色酚酞试液. | 溶液变红. | 我的猜想成立 |
3.小明的妈妈总是膝盖疼,医生说她骨质疏松,需要补钙,下列食品中不适合的是( )
| A. | 小白菜 | B. | 虾皮 | C. | 豆浆 | D. | 牛奶 |
20.如表整理的与化学有关的知识不完全正确的一组是( )
| A | 性质与用途 | B | 食品保鲜的办法 |
| 氢气燃烧产物为水--最理想的燃料 金刚石硬度大--钻探机钻头 一氧化碳具有还原性--冶炼金属 | 填充氮气--防止变质 放入生石灰--防止受潮 放入细铁粉--防止受潮和变质 | ||
| C | 生活常识 | D | 环保与物质的利用 |
| 取暖防中毒--煤炉上放一壶水 防菜刀生锈--喷水后悬挂起来 海鲜品保鲜--甲醛水溶液浸泡 | 减少水污染--使用无磷洗衣粉 减少汽车尾气污染--使用乙醇汽油 减少酸雨的发生--使用新型能源 |
| A. | A | B. | B | C. | C | D. | D |
7.下列有关微粒的说法错误的是( )
| A. | 原子、分子、离子都是构成物质的微粒 | |
| B. | 钠原子失去1个电子形成钠离子 | |
| C. | 过氧化氢分子由氢分子和氧分子组成 | |
| D. | 分子是在不停地运动 |
17.下列各组物质中,均属于纯净物的是( )
| A. | 合成纤维、维生素 | B. | 天然气、水银 | C. | 冰水混合物、干冰 | D. | 液态氮、碘盐 |
1.如表是元素周期表的一部分,请根据表中提供的信息按要求填空.
(1)元素①是Al(填元素符号);由6、8、11号三种元素组成的物质化学式为Na2CO3.
(2)由元素②组成的单质在空气中燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)请画出原子序数是9的元素的原子结构示意图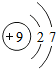 ,化学反应中该元素的原子易得到电子(填“得到”或“失去”),形成阴离子(填“阴”或“阳”).
,化学反应中该元素的原子易得到电子(填“得到”或“失去”),形成阴离子(填“阴”或“阳”).
(4)在元素周期表中,同一周期的元素最外层电子数的变化规律是:从左到右随着核电荷数的依次递增最外层电子数依次增多.
| 3 Li 锂 | 4 Be 铍 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 11 Na 镁 | 12 Mg 镁 | ① | 14 Si 硅 | ② | 16 S 硫 | 17 Cl 氯 | 18 Ar 氩 |
(2)由元素②组成的单质在空气中燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)请画出原子序数是9的元素的原子结构示意图
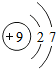 ,化学反应中该元素的原子易得到电子(填“得到”或“失去”),形成阴离子(填“阴”或“阳”).
,化学反应中该元素的原子易得到电子(填“得到”或“失去”),形成阴离子(填“阴”或“阳”).(4)在元素周期表中,同一周期的元素最外层电子数的变化规律是:从左到右随着核电荷数的依次递增最外层电子数依次增多.
2.下列说法错误的是( )
| A. | 铁丝在氧气中燃烧有黑色固体生成 | |
| B. | 浓硫酸可做干燥剂是因为浓硫酸具有脱水性 | |
| C. | 废水中含有酸性物质必须先用碱性物质中和成中性以后才能排放 | |
| D. | 石墨质软滑腻,能导电、导热、耐高温 |
 据调查,中学生近视眼的概率已达到一半以上,因此青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具.
据调查,中学生近视眼的概率已达到一半以上,因此青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具.