题目内容
2.常用澄清石灰水检验二氧化碳的存在,若二氧化碳过量,二氧化碳又会与碳酸钙、水反应生成易溶的碳酸氢钙[Ca(HCO3)2],【已知:CaCO3+H2O+CO2═Ca(HCO3)2】.向含有氢氧化钙14.8g的石灰水里缓缓通入一定量二氧化碳,充分反应后若生成10g沉淀,则通入二氧化碳的质量可能为4.4g或13.2g.分析 二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,碳酸钙和水、二氧化碳反应生成碳酸氢钙,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:当二氧化碳不足时,设二氧化碳质量为x,
Ca(OH)2+CO2═CaCO3↓+H2O,
44 100
x 10g
$\frac{44}{x}$=$\frac{100}{10g}$,
x=4.4g,
反应的化学方程式及其质量关系如下所示:
Ca(OH)2+CO2═CaCO3↓+H2O,CaCO3+H2O+CO2═Ca(HCO3)2,
74 44 100 100 44
14.8g 8.8g 20g 10g 4.4g
由以上质量关系可知,14.8g氢氧化钙和8.8g二氧化碳反应生成20g碳酸钙,溶解10g碳酸钙需要消耗4.4g二氧化碳,因此当二氧化碳过量时,最终得到10g碳酸钙沉淀,消耗二氧化碳质量为:8.8g+4.4g=13.2g.
故填:4.4;13.2.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
12.实验室常用锌和稀硫酸制取氢气,下列操作错误的是( )
| A. |  稀释浓硫酸 稀释浓硫酸 | B. |  加入锌粒 | C. |  产生氢气 产生氢气 | D. | 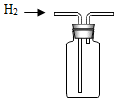 收集氢气 |
10.分类是化学学习的重要方法之一,按单质、氧化物混合物的顺序排列的一组物质是( )
| A. | 金刚石、四氧化三铁、冰水混合物 | B. | 液氧、干冰、洁净的空气 | ||
| C. | 冰、氧化汞、石灰石 | D. | 氦气、氯酸钾、乙醇汽油 |
17.下列关于CO2与CO的不同点比较错误的是( )
| A. | 组成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子 | |
| B. | 性质:CO2能溶于水,水溶液呈酸性;CO难溶于水,但能燃烧 | |
| C. | 用途:CO2可用于光合作用、灭火等;CO可作气体燃料,还可用于人工降雨 | |
| D. | 危害:CO2会造成“温室效应”;CO易与血液中的血红蛋白结合引起中毒 |
7.运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是( )
| A. | 钠原子和钠离子的化学性质相似 | |
| B. | 水和过氧化氢的组成元素相同,则两者的化学性质相同 | |
| C. | 同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率 | |
| D. | Na+、Mg2+、Cl-的最外层电子数均为8,由此得出离子的最外层电子数均为8 |
14.在氧化铁(Fe2O3)、氧化亚铁(FeO)和四氧化三铁(Fe3O4)和硫化亚铁(FeS2)这四种铁的化合物中,铁的质量分数按由大到小顺序排列的是( )
| A. | Fe3O4、Fe2O3、FeS2、FeO | B. | FeO、FeS2、Fe2O3、Fe3O4 | ||
| C. | FeO、Fe3O4、Fe2O3、FeS2 | D. | FeS2、Fe2O3、Fe3O4、FeO |
18.要善于从化学的视角认识世界.对下列事实解释错误的是( )
| 选项 | 事实 | 解释 |
| A | 墙内开花墙外香 | 分子在不断运动 |
| B | 50L水和50L酒精混合后的体积小于100L | 分子之间有间隔 |
| C | 水蒸发变成水蒸气 | 分子大小发生改变 |
| D | N2的化学性质不活泼,O2的化学性质比较活泼 | 不同分子性质不同 |
| A. | A | B. | B | C. | C | D. | D |

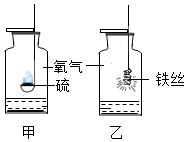 比较甲乙两图中物质在氧气燃烧中的实验,回答下列问题:
比较甲乙两图中物质在氧气燃烧中的实验,回答下列问题: