题目内容
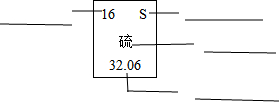
一定质量的锌和50mL密度为1.07g/cm3的稀硫酸(H2SO4),恰好完全反应生成氢气2.24L(标准情况下氢气的密度为0.0899g/L)和硫酸锌(ZnSO4),求参加反应的Zn的质量和该稀硫酸溶液中含纯硫酸的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:由生成氢气的体积、密度,可以计算出生成氢气的质量;由反应的化学方程式可列式计算出参加反应的Zn的质量、该稀硫酸溶液中含纯硫酸的质量,据此进行分析解答.
解答:解:生成氢气的质量为0.0899g/L×2.24L≈0.2g
设参加反应的Zn的质量为x,该稀硫酸溶液中含纯硫酸的质量为y
Zn+H2SO4═ZnSO4+H2↑
65 98 2
x y 0.2g
=
x=6.5g
=
y=9.8g
50mL=50cm3
该稀硫酸溶液中含纯硫酸的质量分数为
×100%≈18.3%.
答:参加反应的Zn的质量为6.5g;该稀硫酸溶液中含纯硫酸的质量分数为18.3%.
设参加反应的Zn的质量为x,该稀硫酸溶液中含纯硫酸的质量为y
Zn+H2SO4═ZnSO4+H2↑
65 98 2
x y 0.2g
| 65 |
| 2 |
| x |
| 0.2g |
| 98 |
| 2 |
| y |
| 0.2g |
50mL=50cm3
该稀硫酸溶液中含纯硫酸的质量分数为
| 9.8g |
| 1.07g/cm3×50cm3 |
答:参加反应的Zn的质量为6.5g;该稀硫酸溶液中含纯硫酸的质量分数为18.3%.
点评:本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
现对下列9种物质进行分类:①锰酸钾;②氧化铁;③氨气;④液氧;⑤冰水;⑥镁;⑦二氧化碳;⑧空气;⑨水银,下列分类正确的是( )
| A、混合物:④⑤⑧ |
| B、常温下的气态化合物:③⑦ |
| C、单质:④⑦ |
| D、氧化物:①②⑤⑦ |
实验室用氯酸钾和二氧化锰的混合物制取氧气.某同学向10g含钾元素39%的氯酸钾和氯化钾的混合物中加入3g二氧化锰固体,加热到不再产生气体为止,则实验过程中产生氧气的质量为( )
| A、2.55g | B、3.2g |
| C、1.6g | D、7g |
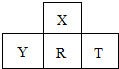 如图是从元素周期表中截取的原子序数1-18的四种不同元素,下列说法错误的是( )
如图是从元素周期表中截取的原子序数1-18的四种不同元素,下列说法错误的是( )| A、元素X比Y、R、T周期数少1 |
| B、Y是金属元素,R是非金属元素,T是稀有气体元素 |
| C、X与R化学性质相似 |
| D、四种元素中,原子序数最大的是T |