题目内容
下表是元素周期表中1-18号元素的排列情况.根据此表进行探究:
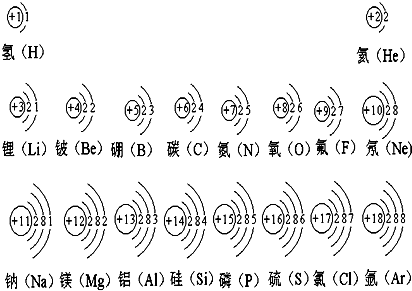
(1)第16号元素的名称是 ,其原子核外的电子层数为 ,它位于第 周期,第 族.
(2)第11号元素属于 元素(填“金属”或“非金属”),它的原子在化学反应中容易 电子(填“得”或“失”),它的离子符号为 .
(3)研究表明:在同一周期中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强.由此推断:第二周期中得电子能力最强的是 原子,失电子能力最强的是 原子,具有稳定结构的是 原子.

(1)第16号元素的名称是
(2)第11号元素属于
(3)研究表明:在同一周期中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强.由此推断:第二周期中得电子能力最强的是
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据周期表中的原子序数来分析元素,然后利用原子结构来回答电子层数;
(2)根据周期表中的原子序数来分析元素,然后利用原子结构中的最外层电子数来分析性质,并书写离子符号;
(3)利用题干的信息分析判断,稳定结构是最外层电子数是8的结构(有一个电子层时最外层电子数是2);
(2)根据周期表中的原子序数来分析元素,然后利用原子结构中的最外层电子数来分析性质,并书写离子符号;
(3)利用题干的信息分析判断,稳定结构是最外层电子数是8的结构(有一个电子层时最外层电子数是2);
解答:解:(1)第16号元素的名称是硫,由表中可以发现其电子层为3层,所以位于第3周期,最外层层电子数为6,故为第六主族;故答案为:硫;3;3;六主
;
(2)第11号元素为钠元素,属于金属元素,因其原子结构中最外层电子数为1,所以在反应中容易失去1个电子,使次外层变成最外层,从而达到稳定结构,钠原子变为钠离子,钠离子带1个单位的正电荷,其符号为Na+,故答案为:金属;失;Na+;
(3)因为从同周期中从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强,所以第二周期中得电子能力最强的是9号元素F,失电子能力最强的应该是3号元素Li,具有稳定结构的原子,最外层一般是8个电子(或只有一个电子层两个电子)的原子,第二周期中元素Ne是具有稳定结构的原子.
故答案为:F、Li、Ne;
;
(2)第11号元素为钠元素,属于金属元素,因其原子结构中最外层电子数为1,所以在反应中容易失去1个电子,使次外层变成最外层,从而达到稳定结构,钠原子变为钠离子,钠离子带1个单位的正电荷,其符号为Na+,故答案为:金属;失;Na+;
(3)因为从同周期中从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强,所以第二周期中得电子能力最强的是9号元素F,失电子能力最强的应该是3号元素Li,具有稳定结构的原子,最外层一般是8个电子(或只有一个电子层两个电子)的原子,第二周期中元素Ne是具有稳定结构的原子.
故答案为:F、Li、Ne;
点评:本题主要考查了学生对元素周期律和元素性质与最外层电子数的关系的认识,元素周期表中,同一周期的元素的原子核外电子层数相同;同一族的元素的原子最外层电子数相同且化学性质相似是解题的关键.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
在下列实验操作(或措施)中,不正确的是( )
| A、用过氧化氢制氧气时,向过氧化氢溶液中加入少量MnO2-加快分解速率 |
| B、点燃氢气前,一定要先检验氢气的纯度-防止发生爆炸 |
| C、装NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞-防止溶液变质 |
| D、实验室储存白磷时,将其浸没在冷水中-防止发生自燃 |
物质在溶解过程中发生两种变化,一种是溶质的分子(或离子)向水中扩散,这一过程吸收热量;另一种是溶质的分子(或离子)和水分子作用,生成水合分子(或水合离子),这一过程放出热量.下列物质溶解在水中时,前一过程明显弱于后一过程的是( )
| A、硝酸铵 | B、氢氧化钠 |
| C、食盐 | D、硝酸钾 |
下列各组离子能共存的是( )
| A、H+、Na+、NO3- |
| B、Ba2+、OH-、SO42- |
| C、Ca2+、NO3-、CO32- |
| D、Ag+、Na+、Cl- |
已知某物质的化学式为R2O3,O元素的质量分数是30%.则R元素的相对原子质量是( )
| A、16 | B、24 | C、27 | D、56 |
 市场上有些食品装在充满气体的塑料袋内,显得鼓鼓的.经询问得知:这样充气的包装,主要是为了使食品能较长时间保鲜、保质和不易压碎.那么,这是什么气体呢?
市场上有些食品装在充满气体的塑料袋内,显得鼓鼓的.经询问得知:这样充气的包装,主要是为了使食品能较长时间保鲜、保质和不易压碎.那么,这是什么气体呢?