题目内容
14. 如图是向50g溶质质量分数为8.0%的氢氧化钠溶液中加入溶质质量分数为10%的稀硫酸至过量的pH变化曲线图,根据图回答以下问题:
如图是向50g溶质质量分数为8.0%的氢氧化钠溶液中加入溶质质量分数为10%的稀硫酸至过量的pH变化曲线图,根据图回答以下问题:(1)A点时,溶液中的含有的阴离子是OH-和SO4 2-;
(2)求恰好反应时消耗稀硫酸的质量.
分析 根据图可以看出是向50g溶质质量分数为8.0%的氢氧化钠溶液中加入溶质质量分数为10%的稀硫酸至过量,A点时显示碱性,为氢氧化钠过量,而B点时pH=7恰好完全反应,根据氢氧化钠的质量和对应的化学方程式求算稀硫酸中溶质的质量.
解答 解:在A点时,pH大于7,为氢氧化钠有剩余,所以此时的溶质为剩余的氢氧化钠和生成的硫酸钠,对应的阴离子的化学式为OH-和SO4 2-;
由于50g溶质质量分数为8.0%的氢氧化钠溶液中含有的氢氧化钠的质量为50g×8.0%=4g
设稀硫酸中溶质的质量为x
2NaOH+H2SO4=Na2SO4+2H2O
80 98
4g x
$\frac{80}{98}$=$\frac{4g}{x}$
x=4.9g
答:(1)A点时,溶液中的含有的阴离子是 OH-和SO4 2-;
(2)恰好反应时消耗稀硫酸的质量是4.9g.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
5.如图为甲、乙两种物质的溶解度曲线.下列说法正确的是( )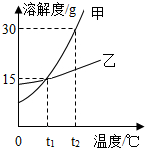

| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t1℃时,甲、乙两种物质的饱和溶液中溶质的质量分数均为15% | |
| C. | 要使接近饱和的乙溶液转化为饱和溶液,可以采用蒸发溶剂的方法 | |
| D. | t2℃时,将50 g甲物质放入100 g水中,得到的溶液的质量为150 g |
3.除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案可行的是( )
| A. | 木炭粉(氧化铜)--加入足量稀硫酸,过滤、洗涤、干燥 | |
| B. | 氯化钠溶液(氯化钙)--通入过量的二氧化碳气体,过滤 | |
| C. | 锌粉(铁粉)--加入足量氯化锌溶液,过滤、洗涤、干燥 | |
| D. | 氢气(氯化氢)--依次通过足量的NaOH溶液和浓硫酸 |
 将104g由氯化钠和氯化钡组成的固体混合物溶解于足量的水中,向所得溶液中滴加14.2%的硫酸钠溶液,所加硫酸钠溶液的质量与生成沉淀的质量之间的关系如图所示.
将104g由氯化钠和氯化钡组成的固体混合物溶解于足量的水中,向所得溶液中滴加14.2%的硫酸钠溶液,所加硫酸钠溶液的质量与生成沉淀的质量之间的关系如图所示.