题目内容
某化学课外活动小组进行了一系列的实验,请按要求作答:
(1)按要求从如图1的A-E装置中选择(填装置的序号).甲同学要用石灰石和盐酸反应制取并收集CO2应选择 ;乙同学要收集一瓶O2,应选择 .

(2)小松同学使用图2装置制取CO2,现有①Na2CO3固体;②块状大理石;③稀HCl;④稀H2SO4四种试剂,应选用的试剂是 (填序号);该反应的化学方程式是 ;反应进行过程中,关闭该装置中的止水夹a 后,可以观察到的现象是 .
(3)通常情况下,乙炔(C2H2)是一种无色、无味、密度比空气略小、难溶于水的气体.实验室常用块状固体电石(CaC2)与水直接反应制取乙炔,同时生成氢氧化钙,有关反应的化学方程式为: .如图2所示,实验室制取乙炔,可选用的发生装置是 ,选用的收集装置是 .
(1)按要求从如图1的A-E装置中选择(填装置的序号).甲同学要用石灰石和盐酸反应制取并收集CO2应选择

(2)小松同学使用图2装置制取CO2,现有①Na2CO3固体;②块状大理石;③稀HCl;④稀H2SO4四种试剂,应选用的试剂是
(3)通常情况下,乙炔(C2H2)是一种无色、无味、密度比空气略小、难溶于水的气体.实验室常用块状固体电石(CaC2)与水直接反应制取乙炔,同时生成氢氧化钙,有关反应的化学方程式为:
考点:二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据制取二氧化碳的反应特点和二氧化碳的密度及水溶性来选择制取装置,根据氧气的密度和水溶性选择收集装置;
(2)根据反应的速率和操控的难以程度选择药品.根据装置内压强的改变分析反应现象.
(3)实验室制取乙炔气体:考虑反应物的状态、反应条件和生成的气体的密度、水溶性;根据反应物,推测生成物,正确书写化学方程式;
(2)根据反应的速率和操控的难以程度选择药品.根据装置内压强的改变分析反应现象.
(3)实验室制取乙炔气体:考虑反应物的状态、反应条件和生成的气体的密度、水溶性;根据反应物,推测生成物,正确书写化学方程式;
解答:解:
(1)甲同学要用石灰石和盐酸反应制取并收集CO2应选择固体和液体不需要加热型反应装置,收集二氧化碳用向下排空气法,因为二氧化碳密度比空气大,能溶于水,收集氧气可用向上排空气法或排水法,因为氧气密度比空气大且不易溶于水;
(2)块状大理石可放在有空的塑料板上,酸要用盐酸,因为硫酸和碳酸钙生成硫酸钙是微溶的,附着在大理石表面,阻止反应进一步进行,反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;反应进行过程中,关闭该装置中的止水夹a后,装置内气压增加,可以观察到试管内液面下降(或长颈漏斗液面上升),反应液与块状固体脱离,反应停止.
(3)电石(主要成分是CaC2)与水反应生成乙炔,同时生成氢氧化钙,化学方程式为:CaC2+2H2O═Ca(OH)2+C2H2↑,反应物是固体和液体,条件不需加热,乙炔密度比空气小,不易溶于水,故发生和收集乙炔的装置组合可以是 B和 C或E.
故答案为:
(1)BD;C或D
(2)②③;CaCO3+2HCl=CaCl2+H2O+CO2↑;试管内液面下降(或长颈漏斗液面上升),反应液与块状固体脱离,反应停止.
(3)CaC2+2H2O═Ca(OH)2+C2H2↑,B; C或E.
(1)甲同学要用石灰石和盐酸反应制取并收集CO2应选择固体和液体不需要加热型反应装置,收集二氧化碳用向下排空气法,因为二氧化碳密度比空气大,能溶于水,收集氧气可用向上排空气法或排水法,因为氧气密度比空气大且不易溶于水;
(2)块状大理石可放在有空的塑料板上,酸要用盐酸,因为硫酸和碳酸钙生成硫酸钙是微溶的,附着在大理石表面,阻止反应进一步进行,反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;反应进行过程中,关闭该装置中的止水夹a后,装置内气压增加,可以观察到试管内液面下降(或长颈漏斗液面上升),反应液与块状固体脱离,反应停止.
(3)电石(主要成分是CaC2)与水反应生成乙炔,同时生成氢氧化钙,化学方程式为:CaC2+2H2O═Ca(OH)2+C2H2↑,反应物是固体和液体,条件不需加热,乙炔密度比空气小,不易溶于水,故发生和收集乙炔的装置组合可以是 B和 C或E.
故答案为:
(1)BD;C或D
(2)②③;CaCO3+2HCl=CaCl2+H2O+CO2↑;试管内液面下降(或长颈漏斗液面上升),反应液与块状固体脱离,反应停止.
(3)CaC2+2H2O═Ca(OH)2+C2H2↑,B; C或E.
点评:实验室装置制取二氧化碳,一般是选用块状大理石和稀HCl,不用大理石和稀硫酸,因为生成的硫酸钙微溶于水,附着在碳酸钙表面,阻止反应继续进行.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
下列属于纯净物的是( )
| A、不锈钢 |
| B、H2O2的水溶液 |
| C、清澈的河水 |
| D、冰糖 |
要将50g溶质质量分数20%的硝酸钾溶液稀释成溶质质量分数为10%的硝酸钾溶液,需加入水的质量为( )
| A、25g | B、40g |
| C、50g | D、100g |
如图所示的四个图象,能正确反映对应变化关系的是( )
A、 水的电解 |
B、 木炭在密闭的容器内燃烧 |
C、 加热一定量的高锰酸钾制氧气 |
D、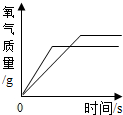 等质量的氯酸钾在有无二氧化锰条件下加热 |
关于催化剂的说法正确的是( )
| A、催化剂自能加快反应的速度 |
| B、催化剂在化学反应前后其质量和化学性质不变 |
| C、催化剂可以增加生成物的质量 |
| D、MnO2可以作为所有化学反应的催化剂 |
为了把校园营造为舒适的学习、生活环境,你认为下列措施不可行的是( )
| A、拒绝外卖进校园 |
| B、露天焚烧垃圾,以减少垃圾的堆积 |
| C、实施绿化工程,多植树、种草 |
| D、学校饭堂的燃料由原来的煤、木炭等改为用电 |
将少量碳酸钠粉末放试管中,可用( )
| A、药匙或纸槽 | B、镊子 |
| C、滴管 | D、另一支试管 |