题目内容
将一瓶盐酸分别倒入两只大烧杯中,将烧杯放在天平两边,并调节天平到指针指在分度盘中间,然后在左盘的烧杯中加10g CaCO3,在右盘的烧杯中加入10g Na2CO3,待烧杯中固体物质完全消失后,天平指针( )
分析:反应物放在一起不反应的状态时,天平是平衡的,指针的偏转主要是看生成二氧化碳的多少,因此解题时判断二氧化碳多少则成为解题的关键所在.由于天平的两托盘的烧杯中分别放入相同质量且足量的稀盐酸,所以可计算相同质量的CaCO3和Na2CO3完全反应放出二氧化碳质量的大小,天平的指针会偏向质量大(下沉)的一方.
解答:解:假设两物质质量均为mg,设mgCaCO3反应放出二氧化碳质量为x,mgNa2CO3反应放出二氧化碳质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
mg x
=
,解之得x=
g
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
mg y
=
,解之得 y=
g,
比较可知等质量的两种碳酸盐完全反应,碳酸钙产生的气体二氧化碳多,质量的增加值偏小,则加入碳酸钙的天平端上升,偏向Na2CO3的一边;
故选:C.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
mg x
| 100 |
| 44 |
| mg |
| x |
| 44m |
| 100 |
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
mg y
| 106 |
| 44 |
| mg |
| y |
| 44m |
| 106 |
比较可知等质量的两种碳酸盐完全反应,碳酸钙产生的气体二氧化碳多,质量的增加值偏小,则加入碳酸钙的天平端上升,偏向Na2CO3的一边;
故选:C.
点评:本题是比较抽象的根据化学方程式的计算,解本题的关键是分析左右两盘实际质量的变化.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案
相关题目
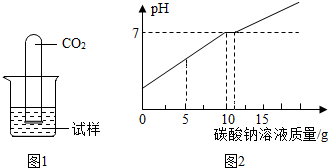
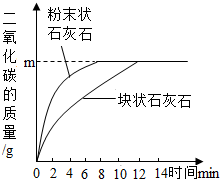 有一种石灰石样品的成分是碳酸钙和二氧化硅(SiO2是一种不溶于水,不与盐酸反应,耐高温的固体),某化学兴趣小组为测定这种石灰石样品中二氧化硅的质量分数,进行了如下实验:
有一种石灰石样品的成分是碳酸钙和二氧化硅(SiO2是一种不溶于水,不与盐酸反应,耐高温的固体),某化学兴趣小组为测定这种石灰石样品中二氧化硅的质量分数,进行了如下实验: