题目内容
某兴趣小组为探究“氧化铁和铜粉”混合物中铜的质量分数,称取一定质量的混合物,按照右图实验装置进行实验:

(1)实验时要“先通一氧化碳气体,后加热”的目的是 。
(2)装置A中发生反应的方程式为 。
(3)实验装置B中的现象是 ,发生反应的化学方程式为 。
(4)该装置的设计有一明显不当之处,你的改进方案是 。
[定量分析]
该兴趣小组按照科学的方案完成实验后,对充分反应后的管内固体X进行如下后续实验探究:

回答下列问题:
(1)写出固体X与稀盐酸反应的方程式: 。
(2)如何证明固体C已经洗涤干净? 。
(3)有色溶液B中含有的溶质: (填化学式)。
(4)根据以上实验流程,计算原混合物“氧化铁和铜粉”中铜的质量分数为 。
(1) 排尽玻璃管内的空气,防止加热时发生爆炸 。
(2) 3CO+ Fe2 O3高温 2Fe + 3CO2
(3) 石灰水变浑浊 ;Ca(OH) 2 + CO2 ==== CaCO 3↓+ H2 O。
(4) 将尾气点燃(用气球收集) 。
[定量分析](1) Fe + 2HCl === FeCl2 + H2 ↑。
(2)取最后的洗涤液滴加紫色石蕊(硝酸银溶液或铁粉或碳酸钠溶液等,其他合理答案即可 。
(3) FeCl2、HCl (填化学式)。(4) 20% 。
【解析】略


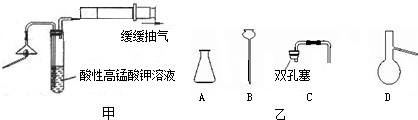
 CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题:
CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题: CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题:
CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题:


