题目内容
潜水艇中需配备氧气再生装置.一般利用Na2O2吸收CO2再生氧气,其反应原理为2Na2O2+2CO2═2Na2CO3+O2.如果一个潜艇兵每天大约需要呼吸12m3的氧气(氧气密度为1.429g/L),需Na2O2的质量为( )A.83596.5g
B.22176g
C.156g
D.17148g
【答案】分析:找出已知和待求,计算出二者的相对分子质量,再根据氧气的质量列比例式计算出过氧化钠的质量即可.
解答:解:氧气的质量=12m3×1.429g/L×1000=17148g
设理论上需要过氧化钠的质量为x.
2Na2O2+2CO2═2Na2CO3+O2
156 32
x 17148g
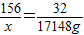
x=83596.5g
故选:A.
点评:解答本题容易出错的地方就是相对分子质量的计算,要注意前面的系数.
解答:解:氧气的质量=12m3×1.429g/L×1000=17148g
设理论上需要过氧化钠的质量为x.
2Na2O2+2CO2═2Na2CO3+O2
156 32
x 17148g
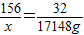
x=83596.5g
故选:A.
点评:解答本题容易出错的地方就是相对分子质量的计算,要注意前面的系数.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案
相关题目