题目内容
20.“气体烙铁”是一种以气体X为燃料的加热仪器,加热温度可达1300℃,反应的化学方程式为2X+13O2$\frac{\underline{\;点燃\;}}{\;}$8CO2+10H2O.燃料X的化学式为( )| A. | C3H8 | B. | C4H10 | C. | CH3OH | D. | CH3COOH |
分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.
解答 解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2X+13O2$\frac{\underline{\;点燃\;}}{\;}$8CO2+10H2O,反应前碳、氢、氧原子个数分别为0、0、26,反应后的生成物中碳、氢、氧原子个数分别为8、20、26,根据反应前后原子种类、数目不变,则2X分子中含有8个碳原子和20个氢原子,则每个X分子由4个碳原子和10个氢原子构成,则物质X的化学式为C4H10.
故选:B.
点评 本题难度不大,掌握利用化学反应前后原子守恒来确定物质的化学式的方法是正确解答此类题的关键.

练习册系列答案
相关题目
10. 如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
 如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )| A. | A点溶液的溶质为NaOH和NaCl | B. | B点溶液的溶质只有NaCl | ||
| C. | a是NaOH溶液质量,b是稀HCl质量 | D. | 该反应是NaOH溶液滴入稀HCl中 |
8.近年来全国多个城市均遭遇了雾霾来袭,下列不可能是雾霾产生的原因的是( )
| A. | 焚烧秸秆 | B. | 汽车尾气 | C. | 光合作用 | D. | 燃烧煤炭 |
15.不同种元素最本质的区别是( )
| A. | 最外层电子数不同 | B. | 中子数不同 | ||
| C. | 质子数不同 | D. | 相对原子质量不同 |
5.下列有关微粒的说法正确的是( )
| A. | 原子通过得失电子形成离子,但离子不能形成原子 | |
| B. | 由分子构成的物质发生化学变化时,分子本身没有改变 | |
| C. | 过氧化氢是由氢原子和氧原子构成的,它与水的组成元素相同 | |
| D. | 原子、分子、离子都是构成物质的微粒,构成物质的微粒在不停地运动 |
12. 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )| A. | t2℃时,甲乙两物质溶液的溶质质量分数一定相等 | |
| B. | 要使接近饱和的乙溶液成为饱和溶液,可蒸发溶剂 | |
| C. | 分别将t2℃甲、乙两种物质的溶液降温至t1℃,一定都有晶体析出 | |
| D. | t1℃时,50g甲的饱和溶液中溶解了10g的甲物质 |
9.分类是化学研究的一种基本方法.农业生产常见的下列四种化合物中,和其他三种物质不属于同一类别的是( )
| A. | NH4NO3 | B. | KNO3 | C. | K2CO3 | D. | Ca(OH)2 |
10.下列关于2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2的说法中,不正确的是( )
| A. | 表示一氧化碳与氧气在点燃条件下反应生成二氧化碳 | |
| B. | 参加反应的一氧化碳与氧气的质量比为28:32 | |
| C. | 反应前后碳原子、氧原子的个数均不变 | |
| D. | 参加反应的氧气与生成的二氧化碳的分子个数比为1:2 |
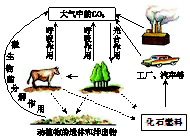 自然界就是一个天然“工厂”.自然界中的物质循环,形成了自然界中物质的平衡.如图所示为自然界中碳循环的示意.
自然界就是一个天然“工厂”.自然界中的物质循环,形成了自然界中物质的平衡.如图所示为自然界中碳循环的示意.