题目内容
6.生活中的下列现象,不包括化学变化的是( )| A. | 牛奶久置后产生酸味 | B. | 新买的家具散发出难闻的气味 | ||
| C. | 铜在空气中久置产生铜绿 | D. | 铁制水龙头滴水处发黄 |
分析 本题考查学生对物理变化和化学变化的确定.判断一个变化是物理变化还是化学变化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成其他物质的是物理变化
解答 解:A、牛奶久置后产生酸味,有酸性物质生成,属于化学变化,故A错;
B、新买的家具散发出难闻的气味,是家居中散发出的甲醛等物质,但不是生成的新物质,属于物理变化,故B正确;
C、铜在空气中久置产生铜绿,是铜与二氧化碳、氧气、水反应生成铜绿,属于化学变化,故C错;
D、铁制水龙头滴水处发黄,是因为铁与氧气、水反应生成了铁锈,属于化学变化,故D错.
故选B.
点评 搞清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在变化中有没有生成其他物质.一般地,物理变化有物质的固、液、气三态变化和物质形状的变化

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.蛇纹石矿可以看做MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验步骤如图所示:
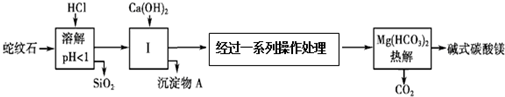
查阅资料:1.几种物质沉淀和溶解时的pH如下表
2.难溶性碱加热会生成两种氧化物,各元素化合价都不变.
探究一:制取碱式碳酸镁
(1)在操作Ⅰ中发生的中和反应是Ca(OH)2+2HCl=CaCl2+2H2O(用化学方程式表示).
(2)进行操作Ⅰ时,需控制溶液pH=6~7,Ca(OH)2不能过量.若Ca(OH)2过量,可能导致Al(OH)3溶解、Mg(OH)2沉淀.
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入NaOH(填入
物质的化学式),然后过滤、洗涤、灼烧(依次填写实验操作名称).
探究二:确定产品碱式碳酸镁(m MgCO3•n Mg(OH)2•x H2O)的组成,组装如图1仪器: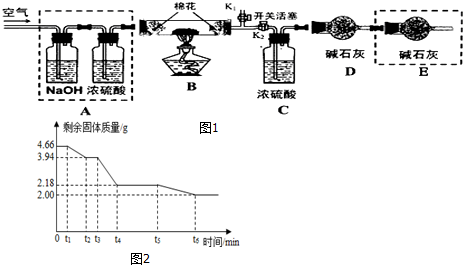
实验测得:硬质玻璃管中剩余的固体质量为2.0g,C处浓H2SO4增重0.9g,D处碱石灰增重1.76g.
(1)仪器连接后,需要进行的操作是检验装置气密性;
(2)A框中装置的作用是除去鼓入空气中的二氧化碳和水蒸气;
(3)通过计算写出碱式碳酸镁的化学式.(请写出计算过程)4MgCO3•Mg(OH)2•4H2O
【交流与反思】
(1)若将E框中的装置去掉,对实验结果的影响是m值偏大,x值偏大(填“偏大”、“偏小”或“不变”)
(2)已知碳酸镁和氢氧化镁在不同的温度下受热易分解为氧化物.为精确测定此碱式碳酸镁受热分解过程中时间与剩余固体质量的关系,结合以上数据,作出图2坐标系,试回答.
①t4~t5时间段固体的化学式为Mg(OH)2和MgO;
②t5~t6时间段发生反应的方程式为Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O.

查阅资料:1.几种物质沉淀和溶解时的pH如下表
| 氢氧化物 | 溶液pH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | 沉淀不溶 | 沉淀不溶 |
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
| Mg(OH)2 | 8.6 | 11.1 | 沉淀不溶 | 沉淀不溶 |
探究一:制取碱式碳酸镁
(1)在操作Ⅰ中发生的中和反应是Ca(OH)2+2HCl=CaCl2+2H2O(用化学方程式表示).
(2)进行操作Ⅰ时,需控制溶液pH=6~7,Ca(OH)2不能过量.若Ca(OH)2过量,可能导致Al(OH)3溶解、Mg(OH)2沉淀.
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入NaOH(填入
物质的化学式),然后过滤、洗涤、灼烧(依次填写实验操作名称).
探究二:确定产品碱式碳酸镁(m MgCO3•n Mg(OH)2•x H2O)的组成,组装如图1仪器:

实验测得:硬质玻璃管中剩余的固体质量为2.0g,C处浓H2SO4增重0.9g,D处碱石灰增重1.76g.
(1)仪器连接后,需要进行的操作是检验装置气密性;
(2)A框中装置的作用是除去鼓入空气中的二氧化碳和水蒸气;
(3)通过计算写出碱式碳酸镁的化学式.(请写出计算过程)4MgCO3•Mg(OH)2•4H2O
【交流与反思】
(1)若将E框中的装置去掉,对实验结果的影响是m值偏大,x值偏大(填“偏大”、“偏小”或“不变”)
(2)已知碳酸镁和氢氧化镁在不同的温度下受热易分解为氧化物.为精确测定此碱式碳酸镁受热分解过程中时间与剩余固体质量的关系,结合以上数据,作出图2坐标系,试回答.
①t4~t5时间段固体的化学式为Mg(OH)2和MgO;
②t5~t6时间段发生反应的方程式为Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O.
11.有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应).现将10g石灰石样品放入烧杯中,再将100g稀盐酸分4次加入烧杯中,每次均充分反应.实验数据记录如下:
求:(1)上述表格中M的值为2
(2)该石灰石样品中碳酸钙的质量分数.
(3)该稀盐酸的溶质质量分数.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
| 充分反应后剩余固体质量/g | 7 | 4 | 2 | M |
(2)该石灰石样品中碳酸钙的质量分数.
(3)该稀盐酸的溶质质量分数.
18.化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图回答问题:
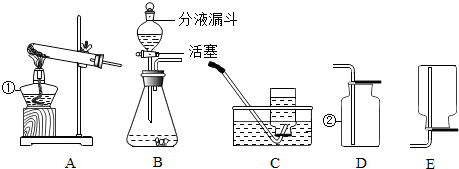
(1)写出标有序号仪器的名称①酒精灯,②集气瓶.
(2)实验室可选用KMnO4制氧气,反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室用大理石和稀盐酸反应制取二氧化碳,可选用的收集装置是D(填字母),检验二氧化碳是否收集满的方法是将燃着的木条放在集气瓶口,木条熄灭,证明集满.
(4)实验室用B装置制取O2时,反应很剧烈,请你提出一条与该实验有关的安全注意事项减慢过氧化氢溶液的滴加速度.
(5)某课外小组,用大理石与盐酸反应制取二氧化碳(大理石中杂质不与盐酸反应).甲、乙、丙三同学分别进行实验,实验数据如下(烧杯的质量为25.0g).
若甲、乙、丙三同学中有一名同学所取的大理石和盐酸恰好完全反应.计算大理石中碳酸钙的质量分数.(计算结果精确到0.1%).

(1)写出标有序号仪器的名称①酒精灯,②集气瓶.
(2)实验室可选用KMnO4制氧气,反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室用大理石和稀盐酸反应制取二氧化碳,可选用的收集装置是D(填字母),检验二氧化碳是否收集满的方法是将燃着的木条放在集气瓶口,木条熄灭,证明集满.
(4)实验室用B装置制取O2时,反应很剧烈,请你提出一条与该实验有关的安全注意事项减慢过氧化氢溶液的滴加速度.
(5)某课外小组,用大理石与盐酸反应制取二氧化碳(大理石中杂质不与盐酸反应).甲、乙、丙三同学分别进行实验,实验数据如下(烧杯的质量为25.0g).
| 烧杯+盐酸 | 大理石 | 充分反应后烧杯+剩余物 | |
| 甲 | 75.0g | 13.2g | 83.8g |
| 乙 | 75.0g | 16.0g | 86.6g |
| 丙 | 95.0g | 13.2g | 103.8g |
15.今年中考化学技能考试中,小林抽到的考题是:用碳酸钠溶液来鉴别稀盐酸、食盐水和澄清石灰水.小林同学按以下过程进行作答:
【进行实验】
写出试管C中反应方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
【发现问题】如何处理上述废液才能减少对环境的污染?
【思考与分析】应先对废液中的溶质成分进行探究,后制定方案.
【实验与探究】
(1)小林将所有废液倒入一洁净烧杯中,静置后得到上层清液.
(2)取少量清液加入适量的氯化钙溶液(中性),再滴加几滴无色酚酞试液,若出现有白色沉淀且酚酞变红的现象,说明上层清液中一定有碳酸钠和氢氧化钠,一定没有Ca(OH)2、HCl.(填化学式)
【方法与应用】通过以上探究,处理上述废液的正确方法是:在废液中继续加入盐酸,调节溶液pH=7,蒸发获得氯化钠晶体.
【进行实验】
| 操作步骤 | 实验现象 | 实验结论 |
| 分别用A、B、C三支试管取样,然后各加入适量碳酸钠溶液 | A中无明显现象 B中有气体 C中有白色沉淀 | A中物质是食盐水 B中物质是稀盐酸 C中物质是澄清石灰水 |
【发现问题】如何处理上述废液才能减少对环境的污染?
【思考与分析】应先对废液中的溶质成分进行探究,后制定方案.
【实验与探究】
(1)小林将所有废液倒入一洁净烧杯中,静置后得到上层清液.
(2)取少量清液加入适量的氯化钙溶液(中性),再滴加几滴无色酚酞试液,若出现有白色沉淀且酚酞变红的现象,说明上层清液中一定有碳酸钠和氢氧化钠,一定没有Ca(OH)2、HCl.(填化学式)
【方法与应用】通过以上探究,处理上述废液的正确方法是:在废液中继续加入盐酸,调节溶液pH=7,蒸发获得氯化钠晶体.
16.通过下列实验,能过达到实验目的是( )
| A. |  如图:制取氧气并检验是否集满 | B. |  如图:验证CO2不支持蜡烛的燃烧 | ||
| C. |  如图:检验醋酸是否具有酸性 | D. | 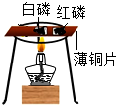 如图:验证白磷的着火点低于红磷 |


