题目内容
20.化学是在原子、分子水平上研究物质及其变化的学科.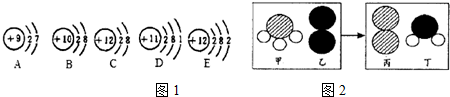
(1)图1是元素周期表中某些元素的原子结构示意图:
①微粒E最外层电子数是2,在化学反应中容易失(填“得”或“失”)电子形成离子,离子符号为Mg2+.
②微粒ABCDE中,属于同种元素的是CE(填编号,下同).
(2)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图2.下列说法正确的是BE.
A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(3)胃酸过多须服用抗酸药.如表为两种抗酸药的有效成分及其构成微粒:
| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg (OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | A13+、Mg2+、OH-、CO32- |
①Mg(OH)2起抗酸作用的微粒是OH-(填微粒符号,下同).
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.则铝碳酸镁起抗酸作用的两种微粒是OH-、CO32-.
分析 (1)①根据最外层的电子数判断元素的性质,写出离子的符号;
②根据质子数决定元素的种类解答;
(2)首先要对模型图进行观察,分析物质的微观构成、物质的类别,再找出物质之间的微粒数目关系,然后再对题中各问加以分析解答.
(3)根据酸碱中和反应、氢离子与碳酸根离子反应等方面进行分析.
解答 解:
(1)①微粒E最外层电子数是2,小于4个,其原子在化学反应中容易失电子形成离子,离子符号是:Mg2+.
②质子数决定元素的种类,微粒ABCDE中,属于同种元素的是CE;
(2)::(1)根据分子式前面的数字表示分子的个数,故“2”表示2个分子的是①;根据元素符号右上角的数字表示离子所带电荷数可知,表示每个微粒带2个单位电荷的是②;
(2)根据反应前后分子变化的微观示意图和质量守恒定律可知,各物质反应的微粒个数关系如下图: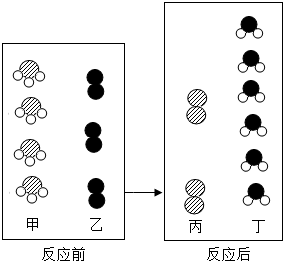
A、由图可知,反应前后一共有3种原子,故A错误;
B、单质是指由同种元素组成的纯净物,故B正确;
C、元素在单质中化合价为零,故反应前后一定有化合价的变化,故C错误;
D、化学变化中分子可再分,但原子不可再分,故D错误;
E、由图可知,甲、丁两种分子的个数比是2:3,故E正确;
故选:BE
(3)胃酸的主要成分为盐酸,①Mg(OH)2中氢氧根离子能与胃酸中的盐酸中的氢离子发生中和反应生成水,从而起到中和胃酸的作用.
②AlMg(OH)3CO3中的OH-、CO32-都能中和胃酸中的氢离子.
故答案为:
(1)①2,失;Mg2+;②CE;
(2)BE
(2)①OH-;②OH-、CO32-.
点评 本题综合性较强,但由于问题较多,容易被弄糊涂了,因此要从概念的科学定义出发,逐一解答.不能光看图示,否则容易出错.了解原子结构示意图与离子结构示意图的区别和联系;掌握核外电子在化学变化中的作用和得失电子的规律特点.

 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案C27H30O16,关于维生素P的叙述中正确的是( )
| A. | 将维生素P在足量的氧气中充分燃烧,产物为CO2和H2O | |
| B. | 维生素P中碳、氢、氧三种元素的质量比为27:30:16 | |
| C. | 维生素P是由27个碳原子、30个氢原子和16个氧原子构成 | |
| D. | 维生素P分子是由碳元素、氢元素和氧元素组成 |
| A. | 铁矿石炼铁 | B. | 干冰致冷 | C. | 海水晒盐 | D. | 风能发电 |
| A. | 向盐酸中滴加硫酸钠溶液 | B. | 向盐酸中滴加酚酞溶液 | ||
| C. | 向氯化镁溶液中滴加氢氧化钾溶液 | D. | 向氯化镁溶液中滴加稀硫酸 |
| A. | 锂具有良好的导电性 | B. | 锂不能与盐酸反应 | ||
| C. | 锂是金属元素 | D. | 锂原子核外有3个电子 |

| A. | 操作时先通CO后加热 | |
| B. | 酒精灯的作用是处理尾气,防止污染空气 | |
| C. | 实验结束时先停止通CO,后停止加热 | |
| D. | 玻璃管里的粉末由红棕色变黑色 |
