题目内容
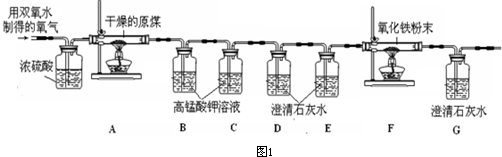
原煤燃烧产生的二氧化硫是造成大气污染的重要原因.二氧化硫又是重要的化工原料,可以生产硫酸,在工业上有重要用途.用硫生产硫酸的总反应可以表示为:2S+3O2+2H2O![]() 2H2SO4.某工厂有含硫0.8%的原煤10000 t,回答下列问题.
2H2SO4.某工厂有含硫0.8%的原煤10000 t,回答下列问题.
(1)如未经处理,完全燃烧会产生污染物二氧化硫________t.
(2)如将所含的硫全部转化为硫酸可以得到纯硫酸多少t?
答案:(1)160;(2)245t
提示:
提示:
|
能够应用质量守恒定律认识元素守恒,能利用方程式对物质质量进行计算 |

练习册系列答案
相关题目