题目内容
在应用固体溶解度的概念时,必须注意以下四点:①指明____________;②溶剂的质量一定是____________;③溶液必须是____________;④溶解度的单位是____________.
解析:
| 温度 100 g 饱和溶液 g
|
提示:

| |||||||
水是宝贵的自然资源,在工农业生产和日常生活中有广泛的应用.

(1)如图a,这种净化水的方法是利用了“水”中各种物质的________不同.(填字母序号)
A.溶解性 B.熔点 C.沸点 D.密度
(2)硬水会给生产和生活带来许多不便,在生活中用
________可以区别硬水和软水.
(3)水是很好的溶剂.下表是KNO3和KCl在不同温度时的溶解度,请回答下列问题:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
②采用任意一种操作方法,将上述烧杯中的剩余固体全部溶解,并将溶液变为不饱和溶液.下列说法中正确的是________(填字母).
A.溶剂质量可能不变 B.溶液中溶质的质量分数一定减小
C.溶液质量一定增大 D.溶液中溶质的质量分数可能增大.
金属材料和水在生产和生活中有着广泛应用.
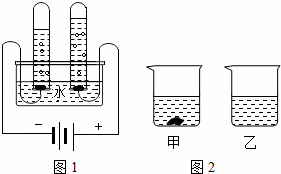
(1)如图1是水的组成测定的实验,此反应的方程式为 .
(2)水是很好的溶剂.下表是KNO3和KCl在不同温度时的溶解度,请回答下列问题:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
|
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
①40℃时,向两个分别盛有45g KNO3和KCl固体的烧杯中,各加入100g的水,充分溶解后,结果如图2所示,则乙烧杯中的溶质是 .
②采用任意一种操作方法,将上述烧杯中的剩余固体全部溶解,并将溶液变为不饱和溶液.下列说法中正确的是 (填字母).
A.溶剂质量可能不变 B.溶液中溶质的质量分数一定增大
C.溶液质量一定增大 D.可采用升温或加水的方法
(3)从下图可知金属具有导热性的是 .
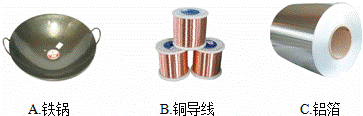
(4)铁制品在空气中会发生锈蚀,其原因是铁与空气中的 共同作用的结果.为防止钢铁制品的锈蚀,厨房中的铁锅和菜刀通常需做的防护是 (要求一种方法即可).
(5)在探究金属的化学性质时,某同学将带锈铁钉放入稀盐酸中,观察到铁锈逐渐消失,溶液由无色逐渐变成黄色,并有气泡产生,有关反应的化学方程式为 、 .
(6)小明向含有FeSO4和CuSO4两种溶质的溶液中,加入一定质量镁粉,待充分反应后,滤液呈浅绿色.根据此现象作出了下列判断,你认为正确的是 (填写序号).
A.滤纸上一定有Cu,可能有Fe,一定没有Mg
B.滤纸上一定有Fe,可能有Mg、Cu
C.滤液中一定有FeSO4,可能有MgSO4、CuSO4
D.滤液中一定有MgSO4、FeSO4,一定没有CuSO4.