题目内容
15. 某盐酸的部分标签如右图所示.欲取该浓溶液配制成1180g 3.7%的稀溶液,其实验步骤为:①计算;②量取100ml的浓盐酸及1062ml水;③溶解.所需仪器:烧杯、玻璃棒、量筒、胶头滴管.
某盐酸的部分标签如右图所示.欲取该浓溶液配制成1180g 3.7%的稀溶液,其实验步骤为:①计算;②量取100ml的浓盐酸及1062ml水;③溶解.所需仪器:烧杯、玻璃棒、量筒、胶头滴管.
分析 利用浓溶液配制稀溶液,采用的加水稀释的方法,由溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
解答 解:取该浓溶液配制成1180g 3.7%的稀溶液,其实验步骤为:①计算,计算所需浓溶液与水的质量;②量取,分别量取浓溶液和水;③溶解.
溶液稀释前后,溶质的质量不变,则所需浓盐酸的体积为x,1.18g/mL×x×37%=1180g×3.7%,x=100mL.
所需水的质量为1180g-1.18g/mL×100mL=1062g(合1062mL).
量筒与胶头滴管用于准确量取浓盐酸和水;烧杯用于完成混匀操作、玻璃棒用于混匀时的搅拌;故所需仪器:烧杯、玻璃棒、量筒、胶头滴管.
故答案为:②100;1062;③量筒、胶头滴管.
点评 本题难度不大,掌握用浓溶液配制稀溶液配制溶质质量分数一定的溶液的基本步骤、溶液稀释前后溶质的质量不变等是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.除去下列物质中的少量杂质,所选试剂及操作都正确的是( )
| 序号 | 物质 | 杂质 | 试剂 | 操作 |
| A | CaO | CaCO3 | 高温煅烧 | |
| B | CO2 | HCl | 足量NaOH溶液 | 洗气 |
| C | NaOH溶液 | Na2CO3 | 适量CaCl2溶液 | 过滤 |
| D | Fe粉 | CuO | 过量盐酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
6.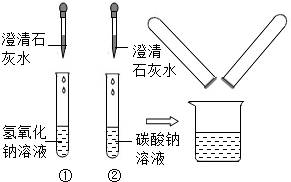 在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如下图所示的实验.
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如下图所示的实验.
(1)写出试管②中碳酸钠与氢氧化钙反应的化学方程式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
【提出问题】滤液中除水外还含有哪些物质?
【猜想】小红认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是氢氧化钠和氢氧化钙(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中小明猜想不合理,请说明理由.Na2CO3和Ca(OH)2能发生反应,不能共存
【实验设计】设计一个简单的实验证明你的猜想正确.
【实验分析】小亮同学针对自己的猜想进行了如下实验:
你认为小亮同学对实验结果判断是否正确?请说明理由不正确,因有氢氧化钠存在,滴入几滴稀盐酸量太少,不会立即出现气泡,但Na2CO3有可能存在
【反思拓展】
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否有剩余
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?在废液中加酸至溶液的pH=7.
 在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如下图所示的实验.
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如下图所示的实验.(1)写出试管②中碳酸钠与氢氧化钙反应的化学方程式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
【提出问题】滤液中除水外还含有哪些物质?
【猜想】小红认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是氢氧化钠和氢氧化钙(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中小明猜想不合理,请说明理由.Na2CO3和Ca(OH)2能发生反应,不能共存
【实验设计】设计一个简单的实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入碳酸钠溶液 | 试管中出现白色浑浊 | 你的猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气泡产生 | 自己的猜想不成立 |
【反思拓展】
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否有剩余
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?在废液中加酸至溶液的pH=7.
3.下列实验事实或实验结论正确的是( )
| A. | 红磷在氧气中燃烧,放出热量,产生大量白雾 | |
| B. | 铁粉与稀硫酸混合后,溶液变为浅绿色且有气体产生 | |
| C. | 硫在氧气中燃烧,产生淡蓝色火焰,生成无色无味的气体 | |
| D. | 酚酞分子运动速率比氨分子运动速率快,所以氨水遇酚酞变红色 |
4.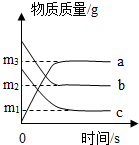 如图是反映某个化学反应里各物质质量与实践的变化关系,下列对比变化的描述中正确的是( )
如图是反映某个化学反应里各物质质量与实践的变化关系,下列对比变化的描述中正确的是( )
 如图是反映某个化学反应里各物质质量与实践的变化关系,下列对比变化的描述中正确的是( )
如图是反映某个化学反应里各物质质量与实践的变化关系,下列对比变化的描述中正确的是( )| A. | 反应后b、c恰好反应,没有剩余 | B. | 物质c的相对分子质量大于b | ||
| C. | m3=m1+m2 | D. | 该反应是化合反应 |
