题目内容
20.有A、B、C、D四种白色粉末(均为纯净物),已知它们是硫酸铜、碳酸钙、氯化钠、硝酸钾中的一种.京京同学进行了实验探究,过程与现象记录如下:第1步:取A、B、C、D四种白色粉末各一药匙,分别加入四支洁净的试管中,各加蒸馏水2毫升,充分振荡后静置.四支试管底部均有固体存在,只有盛放A的试管中液体呈蓝色,其他均呈无色.
第2步:继续向盛放B、C、D的试管中加入适量的稀盐酸,只有盛放D的试管中有气泡产生,其他均无明显变化.
第3步:重新取少量B和C的粉末分别放入另取的2支洁净试管中.各加入适量蒸馏水使其完全溶解,再分别加入几滴硝酸银溶液,结果盛放B的试管中有白色沉淀生成,盛放C的试管中无明显变化.
试回答下列问题:
(1)根据上述实验可知:B是氯化钠.
(2)第1步实验设计的预期现象是“四支试管中只有一支底部有固体存在…”.实验结果是四支试管底部均有固体存在,你认为其余三支试管底部有固体存在的原因可能是溶液达到饱和状态.
(3)写出D与稀盐酸反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
(4)第3步实验为什么不可以在第2步的试管中继续进行,而要重新取样后再继续实验?盐酸中的氯离子会对氯化钠的检验造成干扰.
分析 根据硫酸铜在溶液中显蓝色,碳酸钙难溶于水,碳酸钙和稀盐酸反应会生成二氧化碳气体,氯离子和银离子会生成氯化银沉淀等知识进行分析.
解答 解:硫酸铜在溶液中显蓝色,碳酸钙难溶于水,碳酸钙和稀盐酸反应会生成二氧化碳气体,氯离子和银离子会生成氯化银沉淀,盛放A的试管中液体呈蓝色,其他均呈无色,所以A是硫酸铜,向盛放B、C、D的试管中加入适量的稀盐酸,只有盛放D的试管中有气泡产生,所以D是碳酸钠,B和C的粉末分别放入另取的2支洁净试管中.各加入适量蒸馏水使其完全溶解,再分别加入几滴硝酸银溶液,结果盛放B的试管中有白色沉淀生成,盛放C的试管中无明显变化,所以B是氯化钠,C是硝酸钾,
(1)B是氯化钠;
(2)第1步实验设计的预期现象是“四支试管中只有一支底部有固体存在…”.实验结果是四支试管底部均有固体存在,你认为其余三支试管底部有固体存在的原因可能是:溶液达到饱和状态;
(3)D与稀盐酸的反应是碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)第3步实验不可以在第2步的试管中继续进行,原因是:盐酸中的氯离子会对氯化钠的检验造成干扰.
故答案为:(1)氯化钠;
(2)溶液达到饱和状态;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)盐酸中的氯离子会对氯化钠的检验造成干扰.
点评 在解此类题时,首先分析所给各物质的性质,然后根据题中所给的实验现象进行判断,最后确定各种物质的成分.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
11. 如图提到的“低碳生活”是指生活中要减少能量消耗,从而降低碳特别是二氧化碳的排放.下列做法不属于“低碳生活”方式的是( )
如图提到的“低碳生活”是指生活中要减少能量消耗,从而降低碳特别是二氧化碳的排放.下列做法不属于“低碳生活”方式的是( )
 如图提到的“低碳生活”是指生活中要减少能量消耗,从而降低碳特别是二氧化碳的排放.下列做法不属于“低碳生活”方式的是( )
如图提到的“低碳生活”是指生活中要减少能量消耗,从而降低碳特别是二氧化碳的排放.下列做法不属于“低碳生活”方式的是( )| A. | 广泛使用太阳能和风能等清洁能源 | B. | 尽量使用公共交通工具或步行 | ||
| C. | 大量使用节能技术和节能用具 | D. | 春节期间大量燃放烟花爆竹 |
8.下列关于元素和原子的叙述不正确的是( )
| A. | 元素和原子都是构成物质的基本微粒 | |
| B. | 元素是宏观的抽象概念,无数量意义 | |
| C. | 原子是微观的具体实物,有数量意义 | |
| D. | 元素是核电荷数相同的一类原子的总称 |
15.不饱和溶液在温度不变的条件下,蒸发部分溶剂后又有溶质析出,则对剩余溶液的下列叙述正确的是( )
| A. | 溶液变成饱和溶液 | B. | 溶液仍是不饱和溶液 | ||
| C. | 溶剂的质量与原溶液一样 | D. | 溶质的质量与原溶液一样 |
5. 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如下表:
计算该样品中Na2CO3的质量分数.
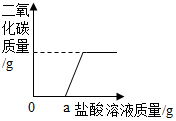
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(选填“大于”、“小于”或“等于”).
 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如下表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(选填“大于”、“小于”或“等于”).
12.用氯化钠配制100g溶质质量分数为20%的氯化钠溶液,现有下列操作:①溶解 ②称取氯化钠 ③过滤 ④量取水 ⑤计算 ⑥蒸发结晶.正确的操作顺序是( )
| A. | ①②③④⑤⑥ | B. | ⑤②④① | C. | ①③⑤④②① | D. | ①③⑥⑤②④① |
