题目内容
(2012?南通)如图是a、b两种固体物质的溶解度曲线.从图中获得的信息错误的是( )
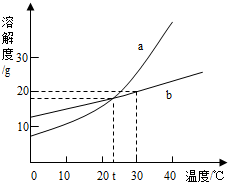

分析:A、根据a物质的溶解度随温度升高而增大分析.
B、从溶解度曲线图可以看出该温度b物质的溶解度为20g分析.
C、根据在t℃时a、b的溶解度相等,饱和溶液溶质质量分数=
×100%分析.
D、根据30℃时,b物质饱和溶液的溶质质量分数=
×100%分析.
B、从溶解度曲线图可以看出该温度b物质的溶解度为20g分析.
C、根据在t℃时a、b的溶解度相等,饱和溶液溶质质量分数=
| 溶解度 |
| 100g+溶解度 |
D、根据30℃时,b物质饱和溶液的溶质质量分数=
| 20g |
| 20g+100g |
解答:解:A、a物质的溶解度随温度升高而增大,A说法正确.
B、从溶解度曲线图可以看出该温度b物质的溶解度为20g,B说法正确.
C、在t℃时a、b的溶解度相等和饱和溶液溶质质量分数=
×100%,溶解度相等所以饱和溶液溶质质量分数相等,C说法正确.
D、30℃时,b物质饱和溶液的溶质质量分数=
×100%=16.7%,D说法不正确.
故选D.
B、从溶解度曲线图可以看出该温度b物质的溶解度为20g,B说法正确.
C、在t℃时a、b的溶解度相等和饱和溶液溶质质量分数=
| 溶解度 |
| 100g+溶解度 |
D、30℃时,b物质饱和溶液的溶质质量分数=
| 20g |
| 20g+100g |
故选D.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.

练习册系列答案
相关题目
(3分)(2012?南通)如图是a、b两种固体物质的溶解度曲线.从图中获得的信息错误的是( )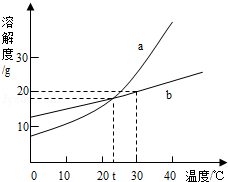
| A.a物质的溶解度随温度升高而增大 |
| B.30℃时,b物质的溶解度为20g |
| C.t℃时,a、b的饱和溶液溶质质量分数相等 |
| D.30℃时,b物质饱和溶液的溶质质量分数为20% |


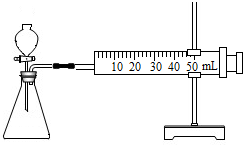 (2012?南通)某化学学习小组为比较镁和铝的金属活动性强弱设计了如下实验方案.
(2012?南通)某化学学习小组为比较镁和铝的金属活动性强弱设计了如下实验方案.