题目内容
【题目】为了探究“水的净化”过程,某实验小组从泽河中去了水样,观察到:A.水样呈黄色,有异味 B.水样浑浊,有固体小颗粒,现对水样进行如下处理:
水样 ![]() 沉降→过滤→吸附
沉降→过滤→吸附 ![]() 自来水
自来水
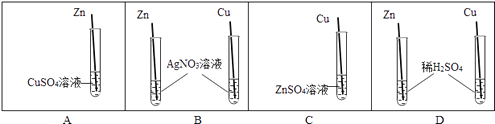
(1)向水样中加入的絮凝剂是 , 搅拌溶液静置一段时间后,进行过滤操作,除去固体小颗粒在化学实验室进行过滤操作,下列仪器(图1)不需要的是 . 
(2)为除去水样中的颜色和异味,向滤液中加入 , 该过程属于变化(填“物理”或“化学”).
(3)通入氯气杀菌消毒得到自来水,发生反应如下:Cl2+H2O=HCl+HClO(次氯酸),其反应的围观过程如图2表示( ![]() 表示氯原子,
表示氯原子, ![]() 表示氧原子,
表示氧原子, ![]() 表示氢原子)
表示氢原子) 
①乙图所示反应的基本类型为;
②上述物质中,属于氧化物的有(填化学式);
③D物质中氯元素的化合价为;
(4)生活中降低水的硬度的方法是 .
(5)用图3的简易净水器处理河水,下面对该净水器分析不正确的是 .
A.能杀菌消毒
B.能把硬水变为软水
C.能得到纯净水.
【答案】
(1)明矾;A
(2)活性炭;物理
(3)分解反应;H2O;+1
(4)煮沸
(5)ABC
【解析】解:(1)由于明矾溶于水的生成物具有吸附性,向水样中加入的絮凝剂是明矾,搅拌溶液静置一段时间后,进行过滤操作,除去固体小颗粒在化学实验室进行过滤操作,由图示可知,过滤用不到的仪器的是酒精灯;(2)为除去水样中的颜色和异味,向滤液中加入活性炭,该过程属于物理变化.(3)①乙图所示反应由一种物质生成了两种物质,基本类型为分解反应;②由物质的构成可知,上述物质中,属于氧化物的是水,化学式是H2O;③由图示可知,D物质是HClO,H的化合价是+1,O的化合价是﹣2,设Cl的化合价是x,则有(+1)+x+(﹣2)=0,x=+1;(4)生活中降低水的硬度的方法是煮沸.(5)A、该净水器不能起到杀菌消毒的作用,错误;B、该净水器不能减少钙、镁离子化合物的含量,不能将硬水变为软水,错误;C、经过该装置得到的水中含有可溶性的杂质,不能得到纯净水,错误;故答为:(1)明矾,A;(2)活性炭,物理;(3)①分解反应;②H2O;③+1;(4)煮沸(5)ABC.
【考点精析】根据题目的已知条件,利用水的净化和从组成上识别氧化物的相关知识可以得到问题的答案,需要掌握水的净化效果由低到高的是静置、吸附、过滤、蒸馏(均为物理方法),其中净化效果最好的操作是蒸馏;既有过滤作用又有吸附作用的净水剂是活性炭;氧化物必须是由两种元素组成,而且是化合物.如:H2O、AI2O3、HCI 都是氧化物,它们也属于化合物,又是纯净物.

【题目】化学小组同学在课外读物中看到:“通常CO2可作灭火剂,但有些物质(如Na)着火,不能用CO2熄灭.”他们决定探究CO2与Na反应的产物.
【提出猜想】CO2与Na反应可能生成4种物质:C、CO、Na2O、Na2CO3 .
【查阅资料】
①Na是非常活泼的金属,常温下与O2、H2O等物质反应.
②碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
③Na2O是白色固体,与H2O反应生成NaOH.
④向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀.
【实验过程】同学们在老师的指导下设计了如图所示装置(部分夹持仪器已略去)
(1)实验记录
序号 | 实验操作 | 主要实验现象 | 实验结论和解释 |
① | 打开a,关闭b,由长颈漏斗注入浓盐酸 | A中产生大量气泡 | E中反应的化学方程式为 |
② | 当E中出现浑浊时,打开b,关闭a,点燃酒精灯 | D中Na剧烈燃烧,产生白烟内壁附着黑色、白色固体 | 反应产物一定有和 |
③ | 取D中白色固体于试管中,加水溶解,再加入石灰水 | 产生白色沉淀 | 反应产物还有 |
(2)实验反思
①实验记录②中,E中出现浑浊,再点燃酒精灯的目的是 .
②装置B中发生的反应的化学方程式是 , 若无装置C,对实验有影响的物质是 .
③检验第4种反应产物是否存在的实验方案:取D中白色固体于试管中,加水溶解, .
(3)数据分析:若在实验过程中至少需要8.8g二氧化碳参加反应,则最少需要含杂质20%的石灰石的质量是多少?(写出计算过程)