题目内容
4. 用如图实验装置进行氯化氢气体与氨气的反应.甲、乙两烧杯里分别盛放浓盐酸和浓氨水,可看到容器中有白烟产生.填空:
用如图实验装置进行氯化氢气体与氨气的反应.甲、乙两烧杯里分别盛放浓盐酸和浓氨水,可看到容器中有白烟产生.填空:(1)产生白烟的化学方程式NH3+HCl=NH4Cl.
(2)盛有浓盐酸的滴管附近白烟更浓,解释产生这一现象的原因:氨分子比氯化氢分子扩散得快.
分析 (1)根据盐酸和氨气反应生成氯化铵固体进行解答;
(2)根据氨分子比氯化氢分子扩散得快进行解答.
解答 解:(1)盐酸和氨气反应生成氯化铵固体,化学方程式NH3+HCl═NH4Cl;
(2)由于氨分子比氯化氢分子扩散得快,所以盛有浓盐酸的烧杯附近白烟更浓.
故答案为:(1)NH3+HCl=NH4Cl;(2)氨分子比氯化氢分子扩散得快.
点评 本题主要考查了微观粒子的特征及其物质之间相互作用时的实验现象和化学方程式的书写等方面的内容.

练习册系列答案
相关题目
14.除去下列物质中的少量杂质,所选试剂或操作不正确的是( )
| 选项 | 物质 | 杂质(少量) | 试 剂 | 操作方法 |
| A | 铜粉 | 氧化铜 | 足量的稀硫酸 | 过滤、洗涤、晾干 |
| B | 氯化钾 | 二氧化锰 | 足量的水 | 过滤 |
| C | 二氧化碳 | 水蒸气 | 浓硫酸 | 洗气 |
| D | 硫酸钡 | 碳酸钡 | 足量的稀盐酸 | 过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
15. 向盛有某液体的烧杯中逐滴加入x溶液至过量(如图1),生成沉淀或气体的质量与加入x溶液的质量关系符合图2的是( )
向盛有某液体的烧杯中逐滴加入x溶液至过量(如图1),生成沉淀或气体的质量与加入x溶液的质量关系符合图2的是( )
 向盛有某液体的烧杯中逐滴加入x溶液至过量(如图1),生成沉淀或气体的质量与加入x溶液的质量关系符合图2的是( )
向盛有某液体的烧杯中逐滴加入x溶液至过量(如图1),生成沉淀或气体的质量与加入x溶液的质量关系符合图2的是( )| 烧杯中的物质 | x溶液 | |
| A | 镁铝合金 | 稀盐酸 |
| B | NaHCO3和NaCl溶液 | 稀盐酸 |
| C | H2SO4和CuSO4溶液 | NaOH溶液 |
| D | 稀盐酸和稀硫酸 | Na2CO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
12.常见原子团的化合价、符号及对应的离子符号
| 原子团 | 符号 | 离子符号 | 化合价 | 原子团 | 符号 | 离子符号 | 化合价 |
| 铵根 | 碳酸根 | ||||||
| 氢氧根 | |||||||
| 硝酸根 | 硫酸根 |
19.被蚊虫叮咬后,人们往往会出现皮肤肿痛.这是因为蚊虫在皮肤内分泌吃的酸性物质(甲酸(CH2O2))对皮肤的刺激作用,下列对甲酸的说法中,错误的是( )
| A. | 甲酸是由碳、氢、氧三种元素组成的 | |
| B. | 甲酸是由甲酸分子构成的 | |
| C. | 一个甲酸分子中含有四个原子 | |
| D. | 甲酸中碳、氢、氧三种原子的个数比为1:2:2 |
16.“阳羡雪芽”是一种绿茶,绿茶中含有单宁酸(化学式为C76H52O46)具有抑制血压上升﹑清热解毒等功效.下列关于单宁酸的说法正确的是( )
| A. | 单宁酸中氧元素的质量分数最小 | |
| B. | 单宁酸由碳﹑氢和氧三种元素组成 | |
| C. | 单宁酸的相对分子质量为1700g | |
| D. | 单宁酸中碳﹑氧两种元素的质量之比为76:46 |
14.某反应的微观示意图如图,有关说法正确的是( )
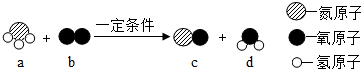

| A. | 该反应属于化合反应 | B. | 氧原子的结构示意图为 | ||
| C. | b,d两种物质均由分子组成 | D. | a物质中氮元素的化合价为+3价 |
 钢铁在生产生活中具有广泛用途.
钢铁在生产生活中具有广泛用途.