题目内容
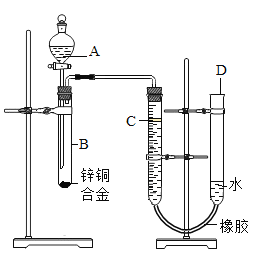
【题目】高新一中化学兴趣小组进行硫酸亚铁铵晶体的热分解实验。小组同学称取此晶体样品39.2g,在科研人员的指导下组装出如图装置时行热分解实验。

(1)[查阅资料]
①硫酸亚铁铵晶体[Fe(NH4)x﹒(SO4)2﹒6H2O,相对分子质量为392]在100°C完全失去结晶水,剩余物在500°C完全分解为铁的某氧化物、SO2、SO3、NH3和H2O。
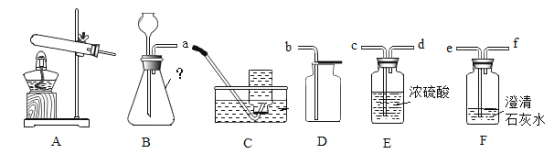
②B装置中浓硫酸只能吸收NH3、SO3和H2O,C装置可以吸收SO2、CO2等气体。
②碱石灰具有吸收水蒸气、二氧化碳气体的作用。
①根据资料内容,硫酸亚铁铵晶体化学式中的x=_____;
②装配好实验装置后,先要_____。
(2)[实验过程]
①实验开始时先能一-段时间N2,分别称量装置B、C的质量。
②控制不同的温度对A中固体加热,并持续通N2。
③停止加热,继续通N2直至装置冷却。
[数据分析]实验过程中测得装置B和C中的质量变化如表。
温度/°C | 室温 | 100 | 500 |
B装置/g | 200 | y | 228 |
C装置/g | 100 | 100 | 103.2 |
①表格中y=_____。
②铁的某氧化物的化学式为_____。
(3)[讨论交流]
加热前后及过程中均需通入N2,停止加热后还要继续通N2至装置冷却的目的是:可以_____和_____。
(4)[实验反思]
如果没有装置:最后盛有碱石灰的干燥管,对C装置数据可能的影响是_____(填“无法确定”、“偏大”、“不变”、“偏小”)。
【答案】2 检查装置气密性 210.8g Fe2O3 除去装置中的空气对实验的影响 防止倒吸和将生成的二氧化硫、三氧化硫、氨气、水蒸气等全部排出 偏大
【解析】
(1)①56+(14+4)×x+96×2+6×18=392,解得x=2.
②装配好实验装置后,先要检查装置的气密性。
(2)[数据分析]
①硫酸亚铁铵晶体的化学式为 (NH4)2Fe(SO4)26H2O,根据题干在100℃时,完全失去结晶水,故39.2g硫酸亚铁铵晶体中将失去39.2g×![]() =10.8g水,都被浓硫酸吸收,故y=210.8g;
=10.8g水,都被浓硫酸吸收,故y=210.8g;
②根据硫酸亚铁铵晶体的化学式为 (NH4)2Fe(SO4)26H2O及反应前的质量为39.2g,求得反应前:铁元素的质量为39.2g×![]() =5.6g,硫元素的质量为6.4g。根据资料显示B装置中浓硫酸只能吸收NH3、SO3和H2O,C装置中氢氧化钠主要用于吸收反应生成的二氧化硫,故装置C质量的增加即为二氧化硫的质量,可知反应生成的二氧化硫的质量为103.2g-100g=3.2g,求得其中硫元素的质量为:3.2g×
=5.6g,硫元素的质量为6.4g。根据资料显示B装置中浓硫酸只能吸收NH3、SO3和H2O,C装置中氢氧化钠主要用于吸收反应生成的二氧化硫,故装置C质量的增加即为二氧化硫的质量,可知反应生成的二氧化硫的质量为103.2g-100g=3.2g,求得其中硫元素的质量为:3.2g×![]() =1.6g,则根据反应前后硫元素的质量是相等的,可知三氧化硫中硫元素的质量为6.4g-1.6g=4.8g,设三氧化硫的质量为x,则
=1.6g,则根据反应前后硫元素的质量是相等的,可知三氧化硫中硫元素的质量为6.4g-1.6g=4.8g,设三氧化硫的质量为x,则![]() ×x=4.8g,解得x=12g;根据题干信息可知,反应生成的气体全部被装置B、C吸收,故剩余的质量为金属氧化物的质量,据此可知铁的氧化物的质量为:39.2g-28g-3.2g=8g,其中铁元素的质量为5.6g,则氧元素的质量为8g-5.6g=2.4g,设该铁的氧化物的化学式为FexOy,则铁元素和氧元素的质量比为56x:16y=5.6g:2.4g,求得x:y=2:3,故铁的氧化物的化学式为Fe2O3。
×x=4.8g,解得x=12g;根据题干信息可知,反应生成的气体全部被装置B、C吸收,故剩余的质量为金属氧化物的质量,据此可知铁的氧化物的质量为:39.2g-28g-3.2g=8g,其中铁元素的质量为5.6g,则氧元素的质量为8g-5.6g=2.4g,设该铁的氧化物的化学式为FexOy,则铁元素和氧元素的质量比为56x:16y=5.6g:2.4g,求得x:y=2:3,故铁的氧化物的化学式为Fe2O3。
(3)[讨论交流]
加热前通入氮气主要是为了除去装置中的空气对实验的影响,过程中继续通N2的目的是将反应生成的气体全部排出,停止加热后继续通N2的目的是防止倒吸。故加热前后及过程中均通入N2,停止加热后继续通N2的目的是防止倒吸和将生成的二氧化硫、三氧化硫、氨气、水蒸气等全部排出
(4)[实验反思]
如果没有装置:最后盛有碱石灰的干燥管,空气中的二氧化碳会被氢氧化钠吸收,故C装置测量结果偏大。

 阅读快车系列答案
阅读快车系列答案