题目内容
 某化学兴趣小组在做Fe和CuSO4溶液反应实验时,发现生成Cu的同时有气泡产生.为了进一步研究做了如下实验:
某化学兴趣小组在做Fe和CuSO4溶液反应实验时,发现生成Cu的同时有气泡产生.为了进一步研究做了如下实验:①取8.5g Fe粉放入一定量的CuSO4中,反应完成后,滤出固体,洗涤、干燥后称量,固体质量为9.2g.
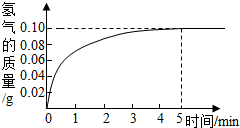
②将9.2g固体与一定质量分数的稀盐酸充分反应,消耗盐酸50.0g,根据实验绘制反应产生氢气的质量与反应时间的关系见图.求:
(1)稀盐酸的质量分数、与稀盐酸反应的Fe的质量.
(2)与CuSO4反应的Fe的质量.
(3)与CuSO4反应的Fe的质量及与盐酸反应的Fe的质量之和
分析:(1)因为铜不与盐酸反应,故产生氢气的反应是Fe与盐酸反应.利用Fe与盐酸反应的化学方程式和生成氢气的质量(由图示数据可知,完全反应后生成氢气的质量为0.10g),列出比例式,就可计算出与稀盐酸反应的Fe的质量和盐酸的质量,然后根据溶质质量分数公式就可计算出稀盐酸的质量分数;
(2)分析题意可知,9.2g固体减去与稀盐酸反应的Fe的质量就是置换出的铜的质量.利用Fe与硫酸铜反应的化学方程式,列出比例式,就可计算出与CuSO4反应的Fe的质量;
(3)计算出“与稀盐酸反应的Fe的质量+与CuSO4反应的Fe的质量”之和,与8.5g比较;根据已知条件和计算出的数据进行分析.
(2)分析题意可知,9.2g固体减去与稀盐酸反应的Fe的质量就是置换出的铜的质量.利用Fe与硫酸铜反应的化学方程式,列出比例式,就可计算出与CuSO4反应的Fe的质量;
(3)计算出“与稀盐酸反应的Fe的质量+与CuSO4反应的Fe的质量”之和,与8.5g比较;根据已知条件和计算出的数据进行分析.
解答:解:(l)设与稀盐酸反应的Fe的质量为x,盐酸的质量为w.
Fe+2HCl═FeCl2+H2↑
56 73 2
x w 0.10g
∴
=
,
=
,
解之得:x=2.8g;w=3.65g;
稀盐酸的质量分数为:
×100%=7.3%;
答:稀盐酸的质量分数为7.3%;与稀盐酸反应的Fe的质量为2.8g;
(2)设与CuSO4反应的Fe的质量为y,
Fe+CuSO4═FeSO4+Cu
56 64
y 9.2g一2.8g
∴
=
,
解之得:y=5.6g;
答:与CuSO4反应的Fe的质量为5.6g;
(3)与CuSO4反应的Fe的质量及与盐酸反应的Fe的质量之和为:2.8g+5.6g=8.4g<8.5g;
在Fe和CuSO4溶液反应实验时,发现生成Cu的同时有气泡产生,而且与CuSO4反应的Fe的质量及与盐酸反应的Fe的质量之和<8.5g,说明有少量Fe与CuSO4溶液中的酸性物质发生了反应,产生了氢气.
故答案为:<;因为有少量Fe与CuSO4溶液中的酸性物质发生了反应.
Fe+2HCl═FeCl2+H2↑
56 73 2
x w 0.10g
∴
| 56 |
| 2 |
| x |
| 0.10g |
| 73 |
| 2 |
| w |
| 0.10g |
解之得:x=2.8g;w=3.65g;
稀盐酸的质量分数为:
| 3.65g |
| 50g |
答:稀盐酸的质量分数为7.3%;与稀盐酸反应的Fe的质量为2.8g;
(2)设与CuSO4反应的Fe的质量为y,
Fe+CuSO4═FeSO4+Cu
56 64
y 9.2g一2.8g
∴
| 56 |
| 64 |
| y |
| 9.2g-2.8g |
解之得:y=5.6g;
答:与CuSO4反应的Fe的质量为5.6g;
(3)与CuSO4反应的Fe的质量及与盐酸反应的Fe的质量之和为:2.8g+5.6g=8.4g<8.5g;
在Fe和CuSO4溶液反应实验时,发现生成Cu的同时有气泡产生,而且与CuSO4反应的Fe的质量及与盐酸反应的Fe的质量之和<8.5g,说明有少量Fe与CuSO4溶液中的酸性物质发生了反应,产生了氢气.
故答案为:<;因为有少量Fe与CuSO4溶液中的酸性物质发生了反应.
点评:本题主要考查学生利用化学方程式和溶质质量分数公式进行计算的能力.学生需根据金属的活动性的知识,分析物质间的反应情况,正确运用化学方程式进行计算.

练习册系列答案
相关题目
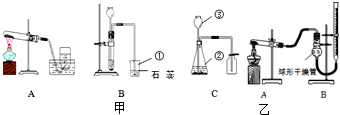
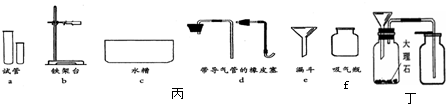
实验室常用下列装置研究气体的制取和性质,根据所学知识回答下列问题.

(1)写出实验室制取氧气的一个化学方程式______,利用该反应制取氧气,发生装置应选______(填序号),组装好实验装置后应进行的操作是______.
(2)一氧化氮气体难溶于水,在空气中容易发生下列反应2NO+O2═2NO2,则收集一氧化氮气体时选用的装置是______(填序号).
(3)按图F做细铁丝在氧气中燃烧的实验,观察到的现象有______.
(4)某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末成分产生浓厚兴趣,并在老师的指导下进行探究活动.
【提出问题】这种单黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成碱和一种气体,在呼吸面具中和潜水艇里常用作供氧剂.
【猜想与探究】猜想:淡黄色粉末可能是:A.硫;B.过氧化钠;C.______(请补充完成猜想C)
探究:过氧化钠与水反应的生成物的成分.
【实验与结论】
| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 | ______ ______ | 猜想A、C不成立 猜想B成立 |
| 探究 | ①用带火星的木条伸入过氧化钠与水反应的试管中 | 木条复燃 | 生成物有______ |
| ②往①试管内的溶液中滴加______ | ______ | 生成物有氢氧化钠 |