题目内容
(7分)某 样品在生产过程中可能含有残余的
样品在生产过程中可能含有残余的 、
、 和
和 三种物质中的一种或几种,现按下图所示进行检验,出现的现象如图中所述。(设过程中所有发生的反应都恰好完全进行,微溶性物质视为完全溶解)
三种物质中的一种或几种,现按下图所示进行检验,出现的现象如图中所述。(设过程中所有发生的反应都恰好完全进行,微溶性物质视为完全溶解)

试根据实验过程和发生的现象,回答下列问题:
(1)沉淀 A 是 (写化学式)
(2)实验步骤①的现象可以说明混进的物质有 (写化学式)
(3)实验证明,溶液 B 中一定存在的溶质是 (写化学式)
(4)实验过程③中发生反应的化学方程式为 。
(5)上述实验现象还不能确认 是否残留在了
是否残留在了 样品中,请你利用溶液D进行实验确认判断:(说明选用试剂、现象和结论) 。
样品中,请你利用溶液D进行实验确认判断:(说明选用试剂、现象和结论) 。
(1) (2)
(2)  (3)
(3) 、
、  (4)
(4)  (5)用试管取少量溶液 D,向其中滴入适量
(5)用试管取少量溶液 D,向其中滴入适量  溶液,(1 分) 若出现白色沉淀,则说明原样品中含有
溶液,(1 分) 若出现白色沉淀,则说明原样品中含有  ; (0.5 分)
; (0.5 分)
【解析】
试题分析:样品中加入氯化钡溶液生成的沉淀A不溶于稀硝酸,则说明样品中一定含有硫酸钠,硫酸钠和氯化钡反应生成的硫酸钡不溶于稀硝酸;溶液B中加入氢氧化钠生成沉淀C,则说明样品中含有氯化镁,氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠;如果要确认是否含有氯化钙,则可以在溶液D中加入碳酸钠溶液,若生成白色沉淀则说明样品中含有氯化钙,反之则不含有氯化钙;
考点:盐的化学性质;化学式;化学方程式;

 智能训练练测考系列答案
智能训练练测考系列答案(11分)小强取回了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的方法,取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下列(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应)请计算:
序号 | 加入稀盐酸质量(g) | 剩余固体质量(g) |
1 | 10 | 5.5 |
2 | 10 | m |
3 | 10 | 1.0 |
4 | 10 | 1.0 |
(1)8g的石灰石样品中含有杂质______克
(2)上表中m的数值=__________
(3)8g石灰石样品完全反应生成二氧化碳多少克?
(14分)钢铁工业是国家工业的基础。
(1)工业上若采用的铁矿石的主要成分为氧化铁,则炼铁的主要反应原理为 (用化学方程式表示),其所用的设备为 ,生铁出口低于炉渣出口的原因是 。
(2)某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究。
【设计实验】用一氧化碳还原纯净的氧化铁粉末,实验装置如图。

【进行实验】该小组按上述实验设计进行实验,实验时应先 (填“通入一氧化碳”或“点燃酒精灯”),目的是: 。
测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量60.0g);
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)。
【分析与讨论】 本实验中,玻璃管内固体粉末由红色全部变为黑色。小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料。
【查阅资料】
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关。
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁。
③
物质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
颜色 | 黑色 | 黑色 | 红色 | 黑色 |
能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
【实验与猜想】
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有 和 。
②进行猜想:黑色固体粉末可能 a.全部为铁 b. c.
【得出结论】 通过实验中获得的数据进行计算,得出黑色固体粉末为 。
【反思与评价】
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高温度和 。
②实验装置图中采用虚线框内的装置,其作用有 和 等。
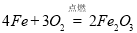
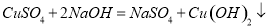
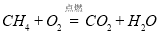
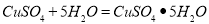
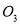 )溶入水中制成的,能脱色去臭,还是很好的杀虫、杀菌剂。下列说法错误的是
)溶入水中制成的,能脱色去臭,还是很好的杀虫、杀菌剂。下列说法错误的是 溶液、
溶液、 溶液、
溶液、 溶液中的各一种,下列四种试剂中,能将上述三种无色溶液一次鉴别出来的是
溶液中的各一种,下列四种试剂中,能将上述三种无色溶液一次鉴别出来的是 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.酚酞试液
溶液 D.酚酞试液