题目内容
13.为了保障宇航员在神舟飞船中有适宜的空气环境,必须处理人体排出的CO2,飞船上采用氢氧化锂(LiOH)作为吸收剂,生成碳酸锂(微溶于水)和水,若每位宇航员每天所呼出的二氧化碳平均约为1.1kg,那么2位宇航员要完成一项为期10天的太空任务,试计算:(1)需要吸收的二氧化碳的质量是:22kg.
(2)在宇宙飞船上至少应携带氢氧化锂的质量.
分析 (1)2位宇航员10天呼出二氧化碳的质量为:1.1kg×2×10=22kg;
(2)根据二氧化碳的质量结合化学方程式可以需要氢氧化锂的质量;
解答 解:(1)2位宇航员10天呼出二氧化碳的质量为:1.1kg×2×10=22kg;故需要吸收的二氧化碳的质量是22kg;
(2)设吸收22kg二氧化碳需要氢氧化锂的质量为x
2LiOH+CO2═Li2CO3+H2O
48 44
x 22kg
$\frac{48}{44}=\frac{x}{22kg}$
x=24kg
答:宇宙飞船上至少应携带氢氧化锂的质量为24kg.
点评 本题主要考查学生运用化学方程式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
8.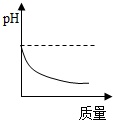 下列操作过程中,溶液pH随加入物质质量变化与如图所示相符的是( )
下列操作过程中,溶液pH随加入物质质量变化与如图所示相符的是( )
 下列操作过程中,溶液pH随加入物质质量变化与如图所示相符的是( )
下列操作过程中,溶液pH随加入物质质量变化与如图所示相符的是( )| A. | 向稀硫酸中逐滴加入氢氧化钠溶液 | B. | 向氢氧化钠溶液中逐滴加水稀释 | ||
| C. | 向水中不断通入氯化氢气体 | D. | 向稀盐酸中加入石灰石 |
18.下列物质充分反应后,所得溶液质量比反应前溶液总质量减小的是( )
| A. | 氧化铁加入稀盐酸中 | B. | 二氧化碳通入足量石灰水中 | ||
| C. | 氢氧化钠溶液和稀盐酸混合 | D. | 碳酸氢钠粉末加入稀盐酸中 |
5.PM2.5指标是指大气中直径小于或等于2.5μm的颗粒物,是空气污染物之一,下列措施对PM2.5的治理不能起积极作用的是( )
| A. | 大力植树造林 | B. | 大力发展火力发电 | ||
| C. | 城市道路定时洒水 | D. | 加强建筑工地扬尘控制 |


 同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化).已知A、H为固体,通常均可在食品包装袋中用于保存食品.人体胃酸中有大量M存在.A、B、C含有两种相同的元素.请回答下列问题:
同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化).已知A、H为固体,通常均可在食品包装袋中用于保存食品.人体胃酸中有大量M存在.A、B、C含有两种相同的元素.请回答下列问题: