题目内容
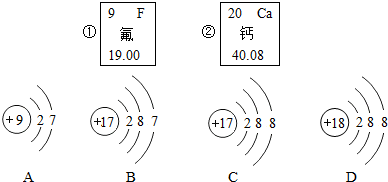
如图中的①、②是氟元素和钙元素在元素周期表中的信息,A、B、C、D是四种微粒的结构示意图.
请回答下列问题:
(1)氟元素的相对原子质量为
(2)四种微粒中属于同种元素的微粒是
(3)A微粒的化学性质与B、C、D中哪一种微粒的化学性质相似
(4)通过观察以上结构示意图请指出属于原子的是
(5)请写出:氟离子符号

请回答下列问题:
(1)氟元素的相对原子质量为
19.00
19.00
,钙元素的原子序数为20
20
(2)四种微粒中属于同种元素的微粒是
BC
BC
(填序号),属于稳定结构的微粒是CD
CD
.(3)A微粒的化学性质与B、C、D中哪一种微粒的化学性质相似
B
B
.(4)通过观察以上结构示意图请指出属于原子的是
ABD
ABD
,阴离子的是C
C
.(5)请写出:氟离子符号
F-
F-
;钙离子的符号Ca2+
Ca2+
.分析:(1)根据氟元素、钙元素在元素周期表中的信息,进行解答.
(2)根据元素的种类由质子数决定,具有最外层8个电子的属于稳定结构,进行解答.
(3)根据元素的化学性质跟它的原子的最外层电子数目有关,最外层电子数相同的元素化学性质相似,进行解答.
(4)根据元素的种类由质子数决定;当核电荷数=质子数=核外电子数,为原子;当核电荷数=质子数>核外电子数,为阳离子;当核电荷数=质子数<核外电子数,为阴离子;当最外层电子数为8(氦是2)时为稳定结构进行解答;
(5)依据两者的最外层电子数特点以及离子符号的书写要求分析解答;
(2)根据元素的种类由质子数决定,具有最外层8个电子的属于稳定结构,进行解答.
(3)根据元素的化学性质跟它的原子的最外层电子数目有关,最外层电子数相同的元素化学性质相似,进行解答.
(4)根据元素的种类由质子数决定;当核电荷数=质子数=核外电子数,为原子;当核电荷数=质子数>核外电子数,为阳离子;当核电荷数=质子数<核外电子数,为阴离子;当最外层电子数为8(氦是2)时为稳定结构进行解答;
(5)依据两者的最外层电子数特点以及离子符号的书写要求分析解答;
解答:解:(1)根据氟元素、钙元素在元素周期表中的信息,氟元素的相对原子质量为19.00,钙元素的原子序数为20;
(2)元素的种类由质子数决定,因为BC的质子数相同,所以BC属于同种元素的粒子;具有最外层8个电子的属于稳定结构,所以是CD属于稳定结构;
(3)根据元素的化学性质跟它的原子的最外层电子数目有关,最外层电子数相同的元素化学性质相似,A粒子的化学性质与B粒子化学性质相似.
(4)A的质子数为9=核外电子数2+7=9,所以A表示原子;B的质子数为17=核外电子数2+8+7=17,所以B表示原子;C的质子数为17<核外电子数2+8+8=18,所以C表示阴离子;D的质子数为18=核外电子数2+8+8=18,所以D表示原子.
(5)氟原子最外层有7个电子,所以化学反应中易得到一个电子,而带一个单位的负电荷,符号为F-;而钙原子最外层含有两个电子,化学变化中易失掉最外层的两个电子从而达到稳定结构,故该粒子会带两个单位的正电荷,符号为Ca2+;
故答案为:(1)19.00;20;(2)BC;CD;(3)B;(4)ABD;C;(5)F-;Ca2+;
(2)元素的种类由质子数决定,因为BC的质子数相同,所以BC属于同种元素的粒子;具有最外层8个电子的属于稳定结构,所以是CD属于稳定结构;
(3)根据元素的化学性质跟它的原子的最外层电子数目有关,最外层电子数相同的元素化学性质相似,A粒子的化学性质与B粒子化学性质相似.
(4)A的质子数为9=核外电子数2+7=9,所以A表示原子;B的质子数为17=核外电子数2+8+7=17,所以B表示原子;C的质子数为17<核外电子数2+8+8=18,所以C表示阴离子;D的质子数为18=核外电子数2+8+8=18,所以D表示原子.
(5)氟原子最外层有7个电子,所以化学反应中易得到一个电子,而带一个单位的负电荷,符号为F-;而钙原子最外层含有两个电子,化学变化中易失掉最外层的两个电子从而达到稳定结构,故该粒子会带两个单位的正电荷,符号为Ca2+;
故答案为:(1)19.00;20;(2)BC;CD;(3)B;(4)ABD;C;(5)F-;Ca2+;
点评:本题难度不大,灵活运用元素周期表中元素的信息、粒子结构示意图的含义是正确解答本题的关键.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目



