题目内容
17.下列实验设计不能达到实验目的是( )| 选项 | A | B | C | D |
| 实验设计 |  |  |  |  |
| 实验目的 | 验证质量守恒定律 | 除去河水中的异味 | 二氧化碳验满 | 比较锌、银的金属活动性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、验证质量守恒定律的实验时,选用药品和装置应考虑:①只有质量没有变化的化学变化才能直接用于验证质量守恒;②如果反应物中有气体参加反应,或生成物中有气体生成,应该选用密闭装置.
B、根据活性炭具有吸附性,能吸附异味和色素,进行分析判断.
C、根据二氧化碳气体的验满方法进行分析判断.
D、在金属活动性顺序中,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,进行分析判断.
解答 解:A、稀盐酸和碳酸钠反应生成二氧化碳气体逸出,反应后烧杯中的物质质量减少,不能直接用于验证质量守恒定律,故选项实验设计不能达到实验目的.
B、活性炭具有吸附性,能吸附异味和色素,用图中装置能除去河水中的异味,故选项实验设计能达到实验目的.
C、检验二氧化碳是否收集满时,应将燃着的木条放在集气瓶口,故选项实验设计能达到实验目的.
D、Zn和Ag分别放入CuSO4溶液中,Zn与CuSO4溶液反应置换出铜,说明了活动性Zn>Cu;Ag与CuSO4溶液不反应,说明了活动性铜>银;由此可得出三种金属活动性锌>铜>银,故选项实验设计能达到实验目的.
故选:A.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体解题时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
7.某金属M的原子量为27,O的原子量为16,已知其金属氧化物中金属M和氧的质量比为9:8,则下列何者为此金属氧化物的化学式?( )
| A. | MO | B. | MO2 | C. | M2O3 | D. | M3O2 |
12.下列基本实验操作不正确的是( )
| A. | 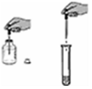 用胶头滴管取液体 | B. | 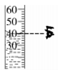 读取液体体积 | ||
| C. | 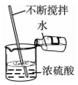 稀释浓硫酸 | D. |  闻气体的气味 |
 随着汽车数量的急剧增加,能源和环保问题日趋严峻.西安街头已出现很多用电力驱动代替燃油的电动汽车,曾被称为“未来汽车”.请结合图示回答下列问题:
随着汽车数量的急剧增加,能源和环保问题日趋严峻.西安街头已出现很多用电力驱动代替燃油的电动汽车,曾被称为“未来汽车”.请结合图示回答下列问题: 将等质量表面积相同的甲、乙两种金属(化合价均为+2)分别放入足量的同一稀盐酸中,经实验测定并绘制出生成氢气好质量与反应时间的关系如图,请回答下列问题:
将等质量表面积相同的甲、乙两种金属(化合价均为+2)分别放入足量的同一稀盐酸中,经实验测定并绘制出生成氢气好质量与反应时间的关系如图,请回答下列问题: 在一次课外小组活动中,同学们从家里收集了一些碎鸡蛋壳和旧电池的锌皮,并制备了澄清石灰水,想利用它们制取某些气体,实验老师给同学们准备了如图所示的仪器和药品:
在一次课外小组活动中,同学们从家里收集了一些碎鸡蛋壳和旧电池的锌皮,并制备了澄清石灰水,想利用它们制取某些气体,实验老师给同学们准备了如图所示的仪器和药品:
