题目内容
某化学探究小组为了测定某种补钙药剂碳酸钙的质量分数,这种补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加入40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据如图2所示.
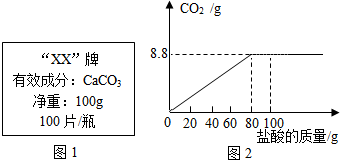
请根据有关信息回答问题:
(1)补钙药剂中的“钙”是指 (填“分子”、“原子”、“离子”或“元素”).
(2)表格中a的数值为 .表中当第4次加入稀盐酸后,其中说明的事实是: .
(3)该品牌补钙药剂中CaCO3的质量分数?

| 第1次 | 第3次 | 第4次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | a | 20 |
(1)补钙药剂中的“钙”是指
(2)表格中a的数值为
(3)该品牌补钙药剂中CaCO3的质量分数?
考点:根据化学反应方程式的计算,元素的概念
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)由元素的概念进行分析解答即可;
(2)由第一次及第四次剩余固体的质量关系,可得到判断:第一次加入的稀盐酸完全反应,剩余固体中含有未反应的碳酸钙,因此可知道每加入20g稀盐酸能消耗5g碳酸钙,则第二加入20g稀盐酸会继续消耗5g碳酸钙,而第三次加入等量稀盐酸时,会继续消耗5g碳酸钙2g,第四次依然如此,而第五次减少了说明此时碳酸钙已完全反应,剩余固体为样品中杂质;
(3)最后剩余的固体为杂质;
(2)由第一次及第四次剩余固体的质量关系,可得到判断:第一次加入的稀盐酸完全反应,剩余固体中含有未反应的碳酸钙,因此可知道每加入20g稀盐酸能消耗5g碳酸钙,则第二加入20g稀盐酸会继续消耗5g碳酸钙,而第三次加入等量稀盐酸时,会继续消耗5g碳酸钙2g,第四次依然如此,而第五次减少了说明此时碳酸钙已完全反应,剩余固体为样品中杂质;
(3)最后剩余的固体为杂质;
解答:解:(1)这里的“钙”是以化合态的性质存在的,指的是钙元素;
(2)由数据记录,第一次加入20g稀盐酸固体质量减少40g-35g=5g,第二次加入同量稀盐酸时,固体质量共减少了35g-5g=30g,第三次剩余固体:30g-5g=25g.故填:25;
表中当第4次加入稀盐酸后,其中说明的事实是80g稀盐酸共消耗20g碳酸钙;
(3)最后剩余的20g固体为该片中的杂质,那么40g该药品中含碳酸钙的质量为:40g-20g=20g,则该品牌补钙冲剂中CaCO3的质量分数是:
×100%=50%;
答:补钙药剂中CaCO3的质量分数50%;
(2)由数据记录,第一次加入20g稀盐酸固体质量减少40g-35g=5g,第二次加入同量稀盐酸时,固体质量共减少了35g-5g=30g,第三次剩余固体:30g-5g=25g.故填:25;
表中当第4次加入稀盐酸后,其中说明的事实是80g稀盐酸共消耗20g碳酸钙;
(3)最后剩余的20g固体为该片中的杂质,那么40g该药品中含碳酸钙的质量为:40g-20g=20g,则该品牌补钙冲剂中CaCO3的质量分数是:
| 20g |
| 40g |
答:补钙药剂中CaCO3的质量分数50%;
点评:由实验数据记录表中剩余固体质量的变化规律,分析反应进行情况,为解决问题的根本,表现出分析实验数据的能力.

练习册系列答案
相关题目
下列关于空气各成分的说法中,错误的是( )
| A、空气中氧气的体积分数约为21% |
| B、氮气化学性质不活泼,可用于食品防腐保鲜 |
| C、空气中的稀有气体一般不跟其他物质反应,又被称为“惰性气体” |
| D、空气质量级别数目越大,空气的质量越好 |
既可以与盐酸反应,又可以与石灰水反应的物质有( )
| A、AgNO3溶液 |
| B、NaOH溶液 |
| C、Na2CO3溶液 |
| D、AgCl |
酸类具有共同化学性质的根本原因是( )
| A、不同的酸的水溶液里都含有相同的H+ |
| B、它们都有酸味 |
| C、不同的酸的水溶液里都含有酸根离子 |
| D、都能使紫色石蕊试液变红色 |
根据物质的用途体现物质的性质这一关系,下列用途体现该物质的性质,说法错误的是( )
| A、金刚石可以刻划玻璃,说明金刚石硬度大 |
| B、一氧化碳可用于工业炼铁,说明一氧化碳具有还原性 |
| C、二氧化碳能使紫色石蕊试液变红,说明二氧化碳具有酸性 |
| D、活性炭可用于防毒面具,说明活性炭具有吸附性 |
下列处理方法不正确的是( )
| A、炒菜时油锅中的油不慎着火,可用锅盖盖灭 |
| B、不慎碰倒酒精灯,酒精在桌面上燃烧起来,应立即用水浇灭 |
| C、扑灭森林火灾的有效方法之一是将大火蔓延路线前的一片树木砍掉,形成隔离带 |
| D、遇到火灾时,可用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区域 |
在空气中,与人类关系最密切的当属氧气.下列关于氧气的说法中,不正确的是( )
| A、带火星的木条在氧气中能够复燃,说明氧气能支持燃烧 |
| B、氧气用于炼钢,目的之一是除去生铁中多余的碳和其他杂质 |
| C、氧气的化学性质非常活跃,但不能与所有的物质发生化学反应 |
| D、用高锰酸钾和氯酸钾制取氧气的反应中,涉及到的MnO2都作催化剂 |