题目内容
反应前整体(含瓶、气球、硫酸、锌)称量,质量为m1,当锌加入后产生H2使气球膨胀,再称量质量为m2,发现m1>m2.
问:
该过程是否符合质量守恒定律?
你如何解释m1>m2?
问:
该过程是否符合质量守恒定律?
符合
符合
.你如何解释m1>m2?
锌和稀硫酸反应后生成氢气,气球膨胀受到空气的浮力大于反应前
锌和稀硫酸反应后生成氢气,气球膨胀受到空气的浮力大于反应前
.分析:运用该装置是密闭装置,该变化是化学变化,生成的氢气不会从装置中跑出去分析.
解答:解:锌和稀硫酸反应生成硫酸锌和氢气,该装置是密闭装置,氢气不会从装置中跑出去,故应该质量相等.但由于反应发生后生成的氢气是气球不断变大,气球受到的浮力就会增大,质量会小于反应前.故答案:符合;锌和稀硫酸反应后生成氢气,气球膨胀受到空气的浮力大于反应前.
点评:本题考查了浮力对反应前后称量结果的影响,浮力大用天平称量的物质的质量就小.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
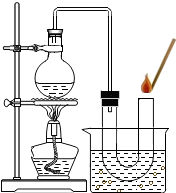 小明将家中清洗伤口用的消毒液--“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
小明将家中清洗伤口用的消毒液--“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.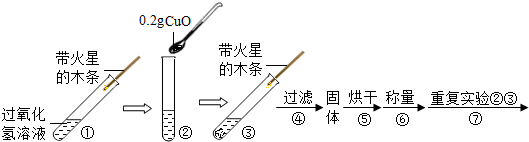
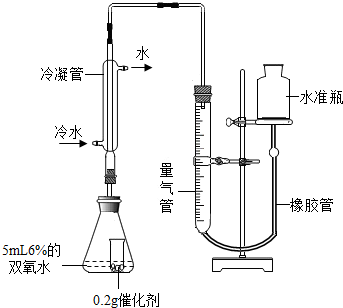 (9)检查该装置气密性的方法是连接好装置,从水准瓶注水,量气管中液面与右边液面形成高度差,做好标记,一段时间后,两边高度差
(9)检查该装置气密性的方法是连接好装置,从水准瓶注水,量气管中液面与右边液面形成高度差,做好标记,一段时间后,两边高度差