题目内容
黑火药的主要成分是硝酸钾、木炭粉、硫磺粉等,点燃时发生爆炸的化学方程式为:2KNO3+S+3C K2S+3CO2↑+X↑,其中X的化学式是( )
K2S+3CO2↑+X↑,其中X的化学式是( )
|
| A. | N2 | B. | NO2 | C. | NO | D. | N2O |
考点:
质量守恒定律及其应用.
专题:
化学用语和质量守恒定律.
分析:
根据化学方程式为S+2KNO3+3C X+K2S+3CO2↑,利用质量守恒定律来分析解答;
X+K2S+3CO2↑,利用质量守恒定律来分析解答;
解答:
解:由化学方程式为S+2KNO3+3C X+K2S+3CO2↑,
X+K2S+3CO2↑,
根据质量守恒定律可知,反应前后元素种类、原子个数相等,
K、O、C、S的原子个数前后相等,
而反应物中有N元素,生成物中应一定有N元素,
则X中只含有N元素,
反应前共2个N原子,则x中共2个N原子
又X的化学计量数为1,则X的化学式为N2,
故选A
点评:
本题考查利用化学方程式来确定某物质的化学式,学生应能根据质量守恒定律中的元素守恒、原子守恒来确定物质的化学式,注意守恒思想在解题中的重要应用.

 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案化学兴趣小组的同学在老师的指导下,开展如下探究活动.
探究一:A、B、C、D分别是纯碱、烧碱、氯化钠、硫酸钠中的一种,它们之间的转化关系如图所示.
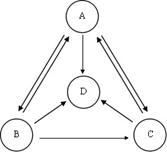
⑴四种物质中,属于碱的是 (填化学式,下同).
⑵物质B是 .
探究二:工业品烧碱含有少量氯化钠杂质。该小组同学从一瓶久置的工业品烧碱样品中取出一定量,在烧杯中加适量水溶解后 得到样品溶液。用稀硫酸与样品溶液做中和反应实验。有关实验操作和现象如下:
得到样品溶液。用稀硫酸与样品溶液做中和反应实验。有关实验操作和现象如下:
| 实验步骤 | 实验现象 |
| Ⅰ向样品溶液中滴加酚酞溶液 | 溶液呈红色 |
| Ⅱ向样品溶液中滴加稀硫酸, 并用玻璃棒 | 滴加一定量稀硫酸后溶液中开始产生气泡 溶液仍呈红色 |
该小组同学对于实验所得红色溶液很感兴趣,展开讨论。溶液里的中和反应是否已经完成?一部分同学认为还没有完成,理由是操作Ⅱ后“溶液仍呈红色”;而另一部分同学则认为中和反应已经完成。结果经过师生共同讨论,确认溶液里中和反应已经完成.
⑶样品溶液的pH 7(填写“<、= 或 >”).
⑷确认溶液里中和反应已经 完成所依据的现象是 .
完成所依据的现象是 .
最后,他们设计一个实验方案,验证了久置的工业品烧碱样品中确实含有氯化钠杂质且已经部分变质,并提纯工业品烧碱。其实验流程及部分实验现象如图所示。
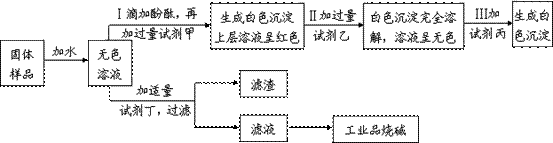
⑸试剂甲和试剂乙的溶液中阴离子都是 (填离子符号).
⑹试剂丁是 (填化学式).
⑺证明工业品烧碱样品已经部分变质的证据是 .
在炼铁工业中,常用石灰石将铁矿石中的杂质二氧化硅转化为炉渣除去,发生反应的化学方程式为:CaCO3+SiO2 X+CO2↑,其中X的化学式是( )
X+CO2↑,其中X的化学式是( )
|
| A. | CaSiO4 | B. | Ca2SiO3 | C. | CaSi2O3 | D. | CaSiO3 |
已知:X和Y两种物质共80g,在一定条件下恰好完全反应,生成Z与W的质量比为11:9,且反应中消耗X的质量是生成W的质量的 ,则反应中消耗Y的质量为( )
,则反应中消耗Y的质量为( )
|
| A. | 16g | B. | 36g | C. | 44g | D. | 64g |
实验室有碳酸钾和碳酸钙的固体混合物75g,使之与500g质量分数为14.6%的盐酸充分反应,将反应后的溶液蒸干得到82.7g固体.则原混合物中金属元素的质量分数为( )
|
| A. | 44% | B. | 46% | C. | 50% | D. | 55% |
 搅拌
搅拌
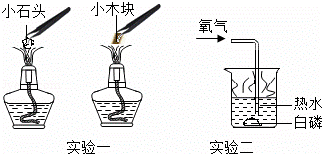
 是____;pH>7的是____(填序号)。
是____;pH>7的是____(填序号)。