题目内容
实验室中有一瓶稀硫酸溶液,小东同学欲测定该硫酸溶液中硫酸的质量分数.小东先取一洁净小烧杯,称其质量为18.2g,然后往其中倒入少量稀硫酸后称量,总质量为38.2g,然后将一枚质量为10.8g的铁钉(已用砂纸打磨除去表面的铁锈)放入该小烧杯中反应,待铁钉表面不再有气泡产生后,再次称量,总质量为48.9g,请回答下列问题:
(1)反应中产生的气体的质量是 .
(2)计算该稀硫酸中硫酸的质量分数是多少?
(3)如果铁钉表面的铁锈未除净,对计算结果的影响是 (选填“偏大”、“偏小”、“无影响”),原因是 .
(1)反应中产生的气体的质量是
(2)计算该稀硫酸中硫酸的质量分数是多少?
(3)如果铁钉表面的铁锈未除净,对计算结果的影响是
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)铁和稀硫酸反应生成硫酸亚铁和氢气,根据质量差可以求生成氢气的质量;
(2)根据氢气的质量求出硫酸中溶质的质量,从而求出废液中硫酸的质量分数即可;
(3)根据铁钉的铁锈未除净,则铁锈消耗一部分硫酸进行解答.
(2)根据氢气的质量求出硫酸中溶质的质量,从而求出废液中硫酸的质量分数即可;
(3)根据铁钉的铁锈未除净,则铁锈消耗一部分硫酸进行解答.
解答:解:(1)完全反应后,容器中的物质的质量差,就是生成氢气的质量,氢气的质量为:38.2g+10.8g-48.9g=0.1g;故填:0.1g;
(2 ) 设与铁反应的硫酸的质量为x,
烧杯中稀硫酸废液的质量为:38.2g-18.2g=20.0g
Fe+H2SO4═FeSO4+H2↑
98 2
x 0.1g
=
x=4.9g
该废液中硫酸的质量分数为:
×100%=24.5%
答:废液中硫酸的质量分数是24.5%;
(3)如果铁钉的铁锈未除净,则铁锈消耗一部分硫酸,氧化铁和硫酸反应生成硫酸铁和水,反应方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;根据氢气求出的硫酸质量就偏小,从而使计算出的硫酸的质量分数偏小.
故填:偏小;铁锈也能消耗一部分硫酸.
(2 ) 设与铁反应的硫酸的质量为x,
烧杯中稀硫酸废液的质量为:38.2g-18.2g=20.0g
Fe+H2SO4═FeSO4+H2↑
98 2
x 0.1g
| 98 |
| x |
| 2 |
| 0.1g |
x=4.9g
该废液中硫酸的质量分数为:
| 4.9g |
| 20.0g |
答:废液中硫酸的质量分数是24.5%;
(3)如果铁钉的铁锈未除净,则铁锈消耗一部分硫酸,氧化铁和硫酸反应生成硫酸铁和水,反应方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;根据氢气求出的硫酸质量就偏小,从而使计算出的硫酸的质量分数偏小.
故填:偏小;铁锈也能消耗一部分硫酸.
点评:本题主要考查化学方程式的书写和有关化学方程式的计算,难度较小,书写化学方程式时要注意四步,一是反应物和生成物的化学式要正确,二是遵循质量守恒定律,三是写上必要的条件,四是看是否有“↑”或“↓”.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目

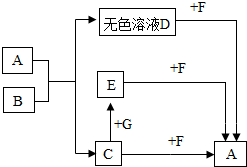 A~G均为初中常见的物质,A是一种常见的建筑材料,其中B是人体胃液中的一种酸,C是植物光合作用所需的一种原料,E是盐,F、G是碱.它们之间有如下图的相互转化关系(图中部分生成物已略去).据此推断:
A~G均为初中常见的物质,A是一种常见的建筑材料,其中B是人体胃液中的一种酸,C是植物光合作用所需的一种原料,E是盐,F、G是碱.它们之间有如下图的相互转化关系(图中部分生成物已略去).据此推断: