题目内容
5.下列曲线能正确表达对应的反应或过程的是( )| A. |  加热一定质量的高锰酸钾固体 | |
| B. |  一定温度下,向饱和KNO3溶液中加入蔗糖固体 | |
| C. | 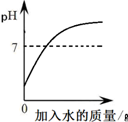 向稀硫酸中不断加水进行稀释 | |
| D. |  相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应 |
分析 根据备选项中反应物和生成物的质量关系进行判断,关键根据题目的表述找清楚那一种物质全部反应,那一种物质有剩余,然后分别对图示的表述是否符合实际情况,特别注意图示的起点和终点的位置.
解答 解:A、高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,所以加热高锰酸钾时,固体质量逐渐减小,然后不变,故A正确;
B、一定温度下,向饱和KNO3溶液中加入蔗糖固体,溶液质量逐渐增大,溶质质量不变,所以溶质质量分数减小,故B错误;
C、向稀硫酸中不断加水进行稀释,只会无限的接近7,不会大于7,故C错误;
D、铁的相对原子质量小,所以相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应,铁生成的氢气多,故D错误.
故选:A.
点评 本题考查了根据图示中两种不同质量物质的反应或者一种物质反应情况来判断生成物、反应物的浓度、剩余物质等随时间或者某种反应物的变化关系;关键是弄清楚图中曲线的变化情况.

练习册系列答案
相关题目
13.硫酸和盐酸是实验室常用的试剂,它们具有相似的化学性质.小华同学在复习有关酸的化学性质时,归纳出以下几点,但并不完整,请你和他一起完成.
(1)
(2)生活中的食醋含有醋酸,用铁锅炒菜时放点食醋,可补充人体需要的微量元素铁,该反应的原理体现了酸的化学性质② (填序号).根据酸的化学性质,再举一例食醋在生活中的应用可除去暖水瓶内的水垢
(3)盐酸、硫酸、醋酸具有相似的化学性质是因为它们的水溶液中都含有氢离子.
(1)
| 酸的化学性质 | 化学方程式举例 |
| ①与酸碱指示剂反应 | |
| ②与多种活泼金属反应 | Mg+H2SO4═MgSO4+H2↑ |
| ③与某些金属氧化物反应 | Fe2O3+6HCl═2FeCl3+3H2O |
| ④与某些盐反应 | CaCO3+2HCl═CaCl2+CO2↑+H2O |
(3)盐酸、硫酸、醋酸具有相似的化学性质是因为它们的水溶液中都含有氢离子.
10.通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分得到粗盐.粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等).
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
[实验方案]某同学为了提纯粗盐,设计了如下实验方案并进行实验.

[交流与表达]
(1)实验步骤①和②的目的是除去粗盐中的难溶性杂质;实验步骤③和④的目的是除去粗盐中的易溶性杂质CaCl2、MgCl2.
(2)实验操作X的名称是过滤,该操作中要用到的玻璃仪器有烧杯、玻璃棒和漏斗.
(3)实验步骤③的主要目的是MgCl2+2NaOH═Mg(OH)2↓+2NaCl (用化学方程式回答);判断氢氧化钠溶液已过量的方法是取样品少许,加入试管中,滴加酚酞试液,溶液变红色.
(4)实验步骤④中生成的沉淀D是碳酸钙.(填写名称)
(5)实验步骤⑤用蒸发溶剂的方法而不用降低溶液温度的方法获取食盐晶体,原因是氯化钠的溶解度受温度影响较小;在蒸发食盐溶液的过程中要使用玻璃棒,作用是搅拌溶液,避免因局部过热,造成液滴飞溅.
[反思与评价]
(6)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中任意一种试剂就能将两种可溶性杂质出去,你认为这种方法不可行(选填“可行”或“不可行”),理由是MgCO3、Ca(OH)2均为微溶物,只用任意一种试剂就会有一种杂质生成微溶物而不能全部除去
(7)有同学认为原实验方案不完善,做出这种评价的依据是在除去MgCl2和CaCl2的同时,又引入了新的杂质NaOH和Na2CO3.
[实验方案设计]
(8)为了完善原实验方案,你设计的实验是向溶液C中逐滴加入稀盐酸至不再产生气泡,滴加酚酞试液时溶液不变色.(仅写出补充部分的实验操作和现象)
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
| 20℃时,一些物质的溶解度 | OH- | CO32- |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |

[交流与表达]
(1)实验步骤①和②的目的是除去粗盐中的难溶性杂质;实验步骤③和④的目的是除去粗盐中的易溶性杂质CaCl2、MgCl2.
(2)实验操作X的名称是过滤,该操作中要用到的玻璃仪器有烧杯、玻璃棒和漏斗.
(3)实验步骤③的主要目的是MgCl2+2NaOH═Mg(OH)2↓+2NaCl (用化学方程式回答);判断氢氧化钠溶液已过量的方法是取样品少许,加入试管中,滴加酚酞试液,溶液变红色.
(4)实验步骤④中生成的沉淀D是碳酸钙.(填写名称)
(5)实验步骤⑤用蒸发溶剂的方法而不用降低溶液温度的方法获取食盐晶体,原因是氯化钠的溶解度受温度影响较小;在蒸发食盐溶液的过程中要使用玻璃棒,作用是搅拌溶液,避免因局部过热,造成液滴飞溅.
[反思与评价]
(6)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中任意一种试剂就能将两种可溶性杂质出去,你认为这种方法不可行(选填“可行”或“不可行”),理由是MgCO3、Ca(OH)2均为微溶物,只用任意一种试剂就会有一种杂质生成微溶物而不能全部除去
(7)有同学认为原实验方案不完善,做出这种评价的依据是在除去MgCl2和CaCl2的同时,又引入了新的杂质NaOH和Na2CO3.
[实验方案设计]
(8)为了完善原实验方案,你设计的实验是向溶液C中逐滴加入稀盐酸至不再产生气泡,滴加酚酞试液时溶液不变色.(仅写出补充部分的实验操作和现象)
14. 如图是碳还原氧化铜的实验,有关说法正确的是( )
如图是碳还原氧化铜的实验,有关说法正确的是( )
 如图是碳还原氧化铜的实验,有关说法正确的是( )
如图是碳还原氧化铜的实验,有关说法正确的是( )| A. | 酒精灯加网罩的作用是防止火焰摆动 | |
| B. | 反应开始的标志是:导管口有气泡产生 | |
| C. | 反应结束的标志是:导管口不再产生气泡 | |
| D. | 实验结束时应先熄灭酒精灯,待试管冷却后再将导管从澄清石灰水中拿出 |
15.下列关于氧气的物理性质的叙述,不正确的是( )
| A. | 通常状态下,是无色无味的气体 | B. | 不易溶于水 | ||
| C. | 液态氧是无色的 | D. | 密度比空气略大 |

