题目内容
如果超细铁粉的质量为5.6g,硫酸铜溶液质量为200g,恰好完全反应.得到不溶固体质量为 .溶液质量为 .
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据题意,由参加反应的铁的质量,由反应的化学方程式计算出生成铜的质量,进而由质量守恒定律,计算出生成溶液的质量.
解答:解:设生成铜的质量为x
Fe+CuSO4═FeSO4+Cu
56 64
5.6g x
=
x=6.4g
溶液质量为5.6g+200g-6.4g=199.2g.
故答案为:6.4g;199.2g.
Fe+CuSO4═FeSO4+Cu
56 64
5.6g x
| 56 |
| 64 |
| 5.6g |
| x |
溶液质量为5.6g+200g-6.4g=199.2g.
故答案为:6.4g;199.2g.
点评:本题难度不大,掌握根据化学方程式的计算、质量守恒定律是正确解答本题的关键.

练习册系列答案
相关题目
浓硫酸和稀硫酸在下列性质上没有明显差异的是( )
| A、腐蚀性 | B、酸性 |
| C、脱水性 | D、吸水性 |
 做氧气的性质探究时,某同学用了如图所示的操作流程.其中A中的黑色固体是木碳.请你猜测:他探究的内容是
做氧气的性质探究时,某同学用了如图所示的操作流程.其中A中的黑色固体是木碳.请你猜测:他探究的内容是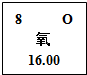 现在已发现的元素有百多种,科学家们根据元素的原子结构和性质,把它们科学有序地排列起来就得到了元素周期表,如图是元素周期表中的一格,你从中获得的信息有(写出两点即可):
现在已发现的元素有百多种,科学家们根据元素的原子结构和性质,把它们科学有序地排列起来就得到了元素周期表,如图是元素周期表中的一格,你从中获得的信息有(写出两点即可):
