题目内容
13.某气体的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量为( )| A. | 64 | B. | 32 | C. | 96 | D. | 16 |
分析 根据n=$\frac{N}{{N}_{A}}$计算该气体的物质的量,再根据M=$\frac{m}{n}$计算该气体的摩尔质量,摩尔质量以g/mol作单位,数值上等于其相对分子质量,进行分析解答.
解答 解:6.4g该气体的物质的量为$\frac{6.02×1{0}^{22}}{6.02×1{0}^{23}×mo{l}^{-1}}$=0.1mol,该气体的摩尔质量为$\frac{6.4g}{0.1mol}$=64g/mol,摩尔质量以g/mol作单位,数值上等于其相对分子质量,故该气体的相对分子质量为64.
故选:A.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
3.中华炭雕(主要成分为木炭),是集观赏与空气净化于一体的工艺品,下列说法错误的是( )
| A. | 炭雕吸附有害气体是物理变化 | B. | 炭雕内部具有疏松多孔的结构 | ||
| C. | 炭雕是质地透明的固体 | D. | 炭雕具有可燃性 |
4.关于原子、分子叙述正确的是( )
| A. | 保持二氧化碳化学性质的微粒是氧原子和碳原子 | |
| B. | 分子是化学变化中的最小微粒 | |
| C. | 水变成水蒸气时,水分子变大 | |
| D. | 臭氧分子是由氧原子构成的 |
1.X、Y、Z三种液体对应的pH如图所示,下列判断正确的是( )

| A. | X一定是盐酸 | B. | Y一定是水 | ||
| C. | Z一定是澄清石灰水 | D. | Z可使紫色石蕊试液变蓝 |
8.下列符号,既能表示一种元素,又能表示这种元素的一个原子,还能表示这种元素的单质的是( )
| A. | Fe | B. | C60 | C. | O | D. | N2 |
5.下列物质的化学式书写正确的是( )
| A. | 碳酸钠NaCO3 | B. | 氢氧化钠Na(OH)2 | C. | 氧化铁O3Fe2 | D. | 硫酸铜CuSO4 |
2.青少年正处于成长期,需要摄入足量钙,这里的“钙”是指( )
| A. | 元素 | B. | 原子 | C. | 分子 | D. | 单质 |
7.下列关于燃烧及事故处理的叙述中正确的是( )
| A. | 室内起火,迅速打开所有门窗通风 | |
| B. | 厨房煤气管道漏气,迅速关闭阀门并开窗通风 | |
| C. | 只有含有碳元素的物质才能燃烧 | |
| D. | 可燃物与氧气接触,就能燃烧 |
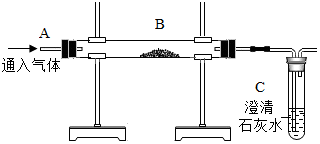 用如图装置完成以下实验:
用如图装置完成以下实验: