题目内容
实验室可用固体过氧化钠和二氧化碳反应制备氧气。化学反应为:过氧化钠+二氧化碳![]() 碳酸钠+氧气
碳酸钠+氧气
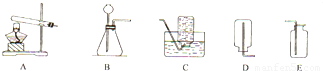
若用图中的装置制取较纯的氧气,试回答下列问题:
(1)装置B的作用是________;
(2)收集氧气应选用的装置是________,检验氧气是否收集满的方法是________。

解析:
| 精析 (1)在二氧化碳与过氧化钠反应转化为氧气的过程中,如果二氧化碳流速太快等原因可能导致二氧化碳反应不充分,而影响制得的氧气的纯度。澄清石灰水则能吸收二氧化碳,除去可能未充分反应的二氧化碳。(2)氧气的密度比空气大,可以用向上排空气法收集,收集时导管应伸入集气瓶的底部,以便除净其中原有的空气。(3)因为氧气能使带火星的木条复燃,所以常用带火星的木条检验氧气。若检验氧气是否收集满,应把带火星的木条放在瓶口,以保证瓶中氧气的纯度不受影响;若区别氧气和其他气体,则可把带火星的木条插入瓶中。
答案 (1)除去可能未充分反应的二氧化碳 (2)D 把带火星的木条放在集气瓶口,若木条复燃,证明氧气已收集满
|
提示:

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案小明参观某养鱼池时,好奇地发现农民向养鱼池中撒一种淡黄色固体——过氧化钙,用来增加鱼池中的含氧量。小明刚学完氧气的实验室制法,于是他想可否用过氧化钙制取氧气。
[提出问题] 过氧化钙可否用于制取氧气?
[查阅资料] 部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气;
能与水反应2CaO2 + 2H2O = 2Ca(OH)2 + O2↑
[猜想与验证]
⑴猜想Ⅰ:加热过氧化钙可制取氧气。小明提出猜想Ⅰ的依据是
。
实验过程:
①检验装置气密性。操作如下:先将导管伸入液面下,用手紧握试管,观察到
,松开手后,导管口有液面上升。
②加入过氧化钙,加热、收集满一瓶气体。
③停止加热。熄灭酒精灯前,应 。
④检验氧气。其方法是 。
实验结论:加热过氧化钙可制取氧气。
⑵ 小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ:实验室可用过氧化钙与水反应制取氧气
实验装置选择 | 实验主要过程 |
| ①检验装置气密性。 ②将水加入过氧化钙中,开始有较多细小气泡放出,随后放出气泡的速度减缓,只收集到极少量气体。该装置放置到第二天,集气瓶中只收集到少量气体,振荡试管后又有少量细小气泡缓慢放出。 |
实验结论: 。
分析与反思:过氧化钙与水反应“开始有较多细小气泡放出,随后放出气泡的速度减缓”的原因可能是 。
(1)实验室制取氧气常用方法有三种:一加热氯酸钾、二是分解过氧化氢溶液、三是 (用化学方程式表示)、
(2)小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体,用来增加鱼池中的含氧量.小明刚学完氧气的实验室制法,于是他想到:
【提出问题】实验室能否用过氧化钙制取氧气?
【查阅资料】过氧化钙[CaO2]是一种淡黄色固体,无臭无味,易受潮,常温下化学性质稳定,在300℃时分解生成氧气,可用做鱼池增氧剂、杀菌剂等.
【猜想与论证】
猜想Ⅰ:实验室可以用加热过氧化钙的方法制取氧气.他的依据是 .
| 实验装置 | 实验主要 |
 | ①检查装置气密性:先将导管口伸入水面下,用受紧握试管,观察到 ,松开后,有少量水进入导管. ②将适量过氧化钙加入试管中,加入,导管口有大量气泡冒出. ③收集一瓶气体并检验气体. ④停止加热,熄灭酒精灯前,应 . |
猜想Ⅱ:实验室中可以用过氧化钙与水反应制取氧气.
| 实验装置 | 实验主要过程 |
| 该实验的发生装置应选择 ,收集装置可选择 或 .(填序号) | ①检验装置气密性. ②将水加入过氧化钙中,有少量细小气泡缓慢放出,该装置放置到第二天,集气瓶中只收集到极少量气体,震荡发生装置仍有少量细小气泡缓慢放出. |
【分析与反思】虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是 .
【知识扩展】小明希望能找到加快过氧化钙与水反应的方法,请你帮他提成一条方便实验验证的建议: .



