题目内容
8.某化学兴趣小组通过查阅资料得知:固体草酸(H2C2O4•2H2O)受热可分解其化学方程式为H2C2O4•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+CO2↑+3H2O,该课题小组的同学在实验室分别进行了如下实验请回答下列问题:
(1)甲同学利用如图装置制取并收集CO:
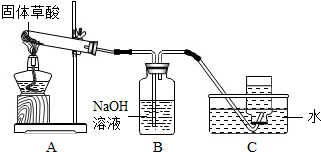
①B装置的作用除去CO2.
②CO集满后,将集气瓶由水槽中加盖取出,然后先将导管从水槽中移出再熄灭酒精灯.
(2)丙同学按如图装置利用草酸分解产生的CO测定某种铁的氧化物的组成.

①当C装置中铁的氧化物全部被还原后,称量剩余的质量为a g,同时测的D装置的质量增加b g,则该铁的氧化物中铁元素和氧元素的质量比为11a:4b.
②丁同学认为去掉A装置,对测定结果无影响,他的观点不正确(填“正确”或“不正确”)你的判断理由是混合气体中的CO2会进入装置,使测定结果不准确.而戊同学认为在D装置后还应再增加某装置,该装置的药品为碱石灰;若无此装置,对测定结果是否有影响?是(填“是”或“否”).
分析 (1)根据草酸分解的产物及实验目的,判断各装置的作用及操作注意事项;二氧化碳与氢氧化钠溶液可反应;
(2)根据对所测装置质量的分析(C装置减少的质量就是氧化物中氧元素的质量),计算铁的氧化物中所含铁元素与氧元素的质量,根据铁的氧化物中铁元素和氧元素的质量比求出氧化物的化学式;分析为测定铁的氧化物的组成各装置的作用,对各装置进行评价,并判断对测定结果所产生的影响.
解答 解:(1)①氢氧化钠溶液属于碱能吸收酸性气体,所以除去二氧化碳;②实验完毕要先撤导管后熄灭酒精灯,防止水倒吸使试管炸裂;故填:除去CO2;将导管从水槽中移出;熄灭酒精灯;
(2)①剩余的质量为a g即铁元素的质量为a g,D装置的质量增加b g即生成二氧化碳质量是b g,由于二氧化碳是一氧化碳还原的结果,所以其中氧元素的一半来自于铁的氧化物,则来自氧化铁的氧元素的质量为$\frac{16b}{44}$,所以氧化铁中铁元素和氧元素的质量比为$\frac{a}{\frac{16b}{44}}$=$\frac{44a}{16b}$=$\frac{11a}{4b}$.
②去掉A装置,对测定结果有影响因为二氧化碳会进入右边的装置内使测量结果不准确.
故答案为:11a:4b;不正确;混合气体中的CO2会进入装置,使测定结果不准确;是.
点评 根据实验目明确所设计的实验装置的作用,是解答好此类题的基础与关键.

练习册系列答案
相关题目
19.下列物质属于氧化物的是( )
| A. | 液氧 | B. | KCl | C. | KClO3 | D. | 干冰 |
13.大蒜中含有一种有效成分辣素“硫化丙烯”,其化学式为C3H6S,能杀菌,具有一定的抗病功能和食疗价值.下列关于硫化丙烯的说法中正确的是( )
| A. | 硫化丙烯中碳元素的质量分数最大 | |
| B. | 硫化丙烯分子由3个碳原子、6个氢原子、1个硫原子构成 | |
| C. | 硫化丙烯由碳、氢、氧三种元素组成 | |
| D. | 硫化丙烯分子中C、H元素原子质量比为2:1 |
1.三种元素的粒子Xm-、Yn+、Zp+都具有相同的电子层结构,已知n>p,则它们的核内质子数(依次用x、y、z表示)的关系为( )
| A. | x=y=z | B. | y>z>x | C. | x>z>y | D. | z>y>x |
18.自然界的水因含有许多杂质而需要净化,下列操作中使水得到净化程度最高的是( )
| A. | 蒸馏 | B. | 活性炭吸附 | C. | 加入肥皂水 | D. | 过滤 |
19.关于饮酒带来的危害逐年增加,股骨头坏死,肝硬化等疾病更是使很多人苦不堪言,关于酒的主要成分乙醇(C2H5OH)下列说法正确的是( )
| A. | 乙醇由三种元素组成,属于混合物 | B. | 乙醇的相对分子质量是45 | ||
| C. | 乙醇中碳氢质量比为4:1 | D. | 一个乙醇分子中含有三个氢分子 |

 如图所示,R是滑动变阻器,它的滑片垂直固定于等臂杠杆中央可左右转动,杠杆两端悬挂等质量体积的铁球,此时杠杆平衡.再将铁球分别同时浸如密度相同的稀硫酸和硫酸铜溶液中.反应一段时间后观察到:
如图所示,R是滑动变阻器,它的滑片垂直固定于等臂杠杆中央可左右转动,杠杆两端悬挂等质量体积的铁球,此时杠杆平衡.再将铁球分别同时浸如密度相同的稀硫酸和硫酸铜溶液中.反应一段时间后观察到: