题目内容
11.写出下列化学符号或符号的意义.(1)2个氢分子2H2
(2)铝元素Al
(3)+3价的铁元素$\stackrel{+3}{Fe}$
(4)2CO22个二氧化碳分子
(5)$\stackrel{+2}{Mg}O$氧化镁中镁元素的化合价为+2价
(6)Na+钠离子.
分析 (1)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(2)书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写.
(3)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.
(4)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(5)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.
(6)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.
解答 解:(1)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2个氢分子可表示为:2H2.
(2)铝元素的元素符号为Al.
(3)由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故+3价的铁元素可表示为:$\stackrel{+3}{Fe}$.
(4)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2CO2可表示2个二氧化碳分子.
(5)由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故$\stackrel{+2}{Mg}$O可表示氧化镁中镁元素的化合价为+2价.
(6)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;Na+可表示钠离子.
故答案为:(1)2H2;(2)Al;(3)$\stackrel{+3}{Fe}$;(4)2个二氧化碳分子;(5)氧化镁中镁元素的化合价为+2价;(6)钠离子.
点评 本题难度不大,掌握常见化学用语(元素符号、分子符号、化合价、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键.

 全能测控期末小状元系列答案
全能测控期末小状元系列答案| A. | X的化学式为HCl | |
| B. | 上述反应属于分解反应 | |
| C. | N2和O2都是空气的成分,其中O2是空气中含量最多的气体 | |
| D. | NH4ClO4中氮元素的质量分数为30% |
(1)金属镁与热水反应的化学方程式为:Mg+2H2O(热)=Mg(OH)2+H2↑.
(2)溶液的红色褪去说明溶液的碱性消失.
(3)据你推测,导致溶液碱性变化的原因是:①氢氧化镁的溶解度随着温度的降低而减小,从而使溶液碱性消失;②吸收了空气中的二氧化碳而使溶液碱性消失.
(4)设计实验来验证你的推测,简要说明操作、现象及结论.
(5)现有Cu与另一种金属(可能是Mg、Fe、Zn中的一种)形成的粉末.现欲测定其组成,进行如下实验:取该粉末16g放入烧杯,将溶质质量分数为14%的稀硫酸280.0g分4次加入该烧杯中,充分反应后,测得剩余的固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70.0 | 70.0 | 70.0 | 70.0 |
| 剩余固体质量/g | 13.6 | 11.2 | 8.8 | 8.4 |
①该粉末中Cu的质量分数.
②该粉末中另一种金属为何种金属?
③第3次加入稀硫酸充分反应后,所得溶液中溶质的质量分数.
| A. | NaNO3、Na2SO4、NH3•H2O | B. | KOH、CuSO4、H2SO4 | ||
| C. | KCl、Ba(NO3)2、HCl | D. | NH4NO3、NaOH、K2SO4 |
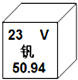 2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13).钒元素的相关信息如图.下列有关钒的说法错误的是( )
2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13).钒元素的相关信息如图.下列有关钒的说法错误的是( )| A. | 相对原子质量为50.94g | B. | 原子的核电荷数是23 | ||
| C. | 元素符号是V | D. | 属于金属元素 |

| A. | H2O | B. | O2 | C. | MgO | D. | HClO |
 眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图:
眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图: