题目内容
9.如图为实验室常用的实验装置,回答问题:
(1)写出带有标号仪器的名称:①锥形瓶;②水槽.
(2)若用A、C装置组合制取氧气,收集氧气完毕时,应先从水中取出导气管(填“熄灭酒精灯”或“从水中取出导气管”),写出A装置中发生反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)写出用B、D装置组合制取氧气的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
分析 (1)根据常用仪器的名称和用途分析解答;
(2)根据实验室用加热氯酸钾、高锰酸钾的方法制取氧气时的注意事项进行分析;根据高锰酸钾分解的反应原理书写化学方程式即可;
(3)根据制取气体的装置来选择制取的方法和原理进行分析.
解答 解:(1)根据常用仪器的名称和用途分析可知两种仪器分别是锥形瓶和水槽;
(2)收集氧气完毕,应先从水中取出导气管,再熄灭酒精灯,防止水倒流入试管,引起试管炸裂;高锰酸钾加热分解生成锰酸钾、氧气和二氧化锰,其化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)B装置适用于固体和液体不需加热制取气体的反应,密度比空气大的气体用向上排空气法收集,通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;氧气的密度比空气的密度大,反应的化学方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
故答案为:(1)①锥形瓶; ②水槽;(2)从水中取出导气管; 2KMnO$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑;(3)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
点评 本题主要考查常用气体装置的选取方法、注意事项以及化学方程式的书写,并考查了学生依据题意获取信息和利用信息处理问题的能力及根据所学知识分析和解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.如图所示,用玻璃杯罩住两支燃烧的蜡烛,一段时间后,下列现象与结论正确的是( )

| A. | 低的蜡烛先灭,因为二氧化碳的密度比空气的密度大 | |
| B. | 高的蜡烛先灭,气体受热膨胀,二氧化碳会上升,聚在玻璃杯的上方 | |
| C. | 该实验说明人从着火的房间逃离时,必须呈站立姿势跑出 | |
| D. | 两只蜡烛同时熄灭,因为玻璃杯中充满了二氧化碳气体 |
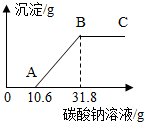 在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验:
在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验: 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.
 课堂上,老师给了同学们一包红色粉未,该粉末可能是铜粉和和氧化铁粉中的一种或两种.为确定该粉末的成分,同学们进行如下探究.请你参与其中并回答问题.
课堂上,老师给了同学们一包红色粉未,该粉末可能是铜粉和和氧化铁粉中的一种或两种.为确定该粉末的成分,同学们进行如下探究.请你参与其中并回答问题.


