题目内容
有一种工业废水,其中含有大量的硫酸亚铁,少量的硫酸铜以及污泥.某同学设计了一个既经济又合理的方法回收铜和硫酸亚铁晶体.方案流程如下:
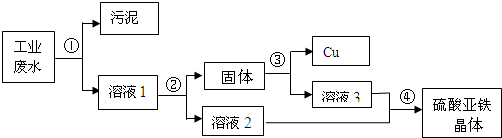
回答下列问题:
(1)操作①是 ,步骤②中:要把硫酸铜完全除去需加入 (填“少量”或“过量”)的铁粉.发生反应的化学方程式是 .
(2)步骤③中:需加入适量的物质是 (填名称),发生反应的化学方程式是 .
(3)步骤④的操作是 .

回答下列问题:
(1)操作①是
(2)步骤③中:需加入适量的物质是
(3)步骤④的操作是
考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据过滤分离不溶性固体与液体,将废水中的污泥与溶液用过滤法分离,得溶液1中含有硫酸铜和硫酸亚铁,加入过量的铁将硫酸铜中的铜全部置换出来,过滤得到铜和铁的混合物和滤液硫酸亚铁,然后在固体混合物中加入适量硫酸与铁反应生成硫酸亚铁溶液,最后将硫酸亚铁溶液蒸发结晶即得硫酸亚铁晶体进行分析.
解答:解:(1)步骤①是将污泥与溶液分离,所以可用过滤,要将硫酸铜与硫酸亚铁的混合溶液中回收铜,同时得到硫酸亚铁溶液,只能加入过量的铁置换硫酸铜溶液中的铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;
(2)铁与硫酸铜反应生成铜和硫酸亚铁,因此经过步骤②之后得到的固体中含有生成的铜和剩余的铁,加入适量稀硫酸与铁反应生成硫酸亚铁,化学方程式为:Fe+H2SO4═FeSO4+H2↑;
(3)将溶液2和3合在一起进行蒸发结晶即可得到硫酸亚铁晶体.
故答案为:(1)过滤,过量,Fe+CuSO4=FeSO4+Cu;
(2)稀硫酸,Fe+H2SO4═FeSO4+H2↑;
(3)蒸发.
(2)铁与硫酸铜反应生成铜和硫酸亚铁,因此经过步骤②之后得到的固体中含有生成的铜和剩余的铁,加入适量稀硫酸与铁反应生成硫酸亚铁,化学方程式为:Fe+H2SO4═FeSO4+H2↑;
(3)将溶液2和3合在一起进行蒸发结晶即可得到硫酸亚铁晶体.
故答案为:(1)过滤,过量,Fe+CuSO4=FeSO4+Cu;
(2)稀硫酸,Fe+H2SO4═FeSO4+H2↑;
(3)蒸发.
点评:从废水中回收金属一般步骤先加入一种廉价金属置换出另一种金属,然后过滤,将过量金属除去即可.

练习册系列答案
相关题目
有X、Y、Z三种金属,将它们分别放入稀硫酸中,发现Y的表面有气泡,X和Z的表面无气泡;将Z放入X的盐溶液中,Z的表面无变化,则三种金属的活动性顺序是( )
| A、X>Y>Z |
| B、Y>X>Z |
| C、Y>Z>X |
| D、Z>Y>X |
下列说法正确的是( )
| A、10%的食盐溶液是指l00 克水中溶解了10克食盐 |
| B、纯碱、烧碱均属碱类 |
| C、某物质只含有一种元素,该物质可能是混合物 |
| D、生铁是化合物 |
下列物质中,不属于溶液的是( )
| A、碘酒 | B、乙醇 |
| C、澄清石灰水 | D、生理盐水 |
“低碳生活”倡导我们在生活中所耗用的能量、材料要尽量减少,从而减低二氧化碳的排放量.下列做法不符合“低碳生活”理念的是( )
| A、教科书循环使用 |
| B、多用电子邮箱、QQ等即时通讯工具 |
| C、鼓励开私家车出行 |
| D、鼓励使用太阳能热水器 |
下列有关配制溶液问题的叙述,正确的是( )
| A、用托盘天平称量固体时,可将固体直接放在托盘天平的托盘上 |
| B、将量好的水倒入烧杯时,烧杯里事先残留了水,不影响所配溶液溶质质量分数的大小 |
| C、将配好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签 |
| D、用浓硫酸配制稀硫酸时,可将水倒入浓硫酸中,并不断搅拌 |
 现有A-F六种常见物质,其中B是食品包装中常用的干燥剂,A、B、C三种白色固体都含有同种金属元素,E是固体单质,D、E、F都含有同种非金属元素.它们的转化关系如图所示.请回答:
现有A-F六种常见物质,其中B是食品包装中常用的干燥剂,A、B、C三种白色固体都含有同种金属元素,E是固体单质,D、E、F都含有同种非金属元素.它们的转化关系如图所示.请回答: