题目内容
某有机物在氧气中充分燃烧后,产物只有二氧化碳和水.甲、乙两组同学分别用
A、B两种方法测定它的组成,如图所示,得到两组数据

请你分析:选用的正确方法是
________,推测出该有机物是由________元素组成,各元素的质量比为________.(实验过程中气体均全部被吸收)
答案:
解析:
解析:
|
B,碳、氢、氧,3∶1∶4 燃烧后的混合气体是 CO2和H2O,A方法中燃烧后的混合气体是通过NaOH溶液吸收CO2同时由于温度降低,部分水蒸气也会留在NaOH溶液中,造成浓H2SO4吸水时,水的质量偏小;B方法中浓H2SO4先吸水测出水的质量,剩余气体CO2,不与浓H2SO4反应,被第2个瓶中的NaOH溶液吸收,测出CO2质量,是正确的方法.混合气体中水的质量m1=153.6g-150g=3.6g,氢元素的质量mH=3.6g×2/18=0.4g;二氧化碳的质量m2=154.4g-150g=4.4g,mC=4.4g×12/44=1.2g,mH+mC=1.6g<2.2g,所以该有机物中含有C、H、O三种元素,其质量比为1.2g∶0.4g∶1.6g=3∶1∶4 |

练习册系列答案
相关题目
某有机物在氧气中充分燃烧后,产生只有二氧化碳和水,甲、乙两组同学分别用下图两种方法测定它的组成.请你分析,并参与测定工作;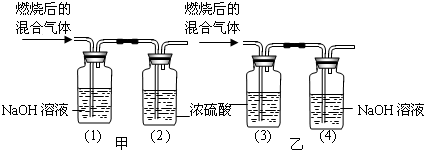
(1)你选用的实验装置是 (“甲”或“乙”),你不选另一个装置的原因是 .
(2)根据表中数据,推测出该有机物是由 元素组成的,各元素的质量比为 (假设实验过程中气体均全部被吸收).
提示:浓硫酸可以吸收水蒸气,氢氧化钠可以吸收二氧化碳.

| 燃烧有机物的质量 | 实验装置 | 实验(1)~(4)装置质量 | ||
| 实验前 | 实验后 | |||
| 甲组 | 1.6g | 甲 | (1)150g | (1)154.6g |
| (2)150g | (1)153.4g | |||
| 乙组 | 1.6g | 乙 | (3)150g | (1)153.6g |
| (4)150g | (1)154.4g | |||
(2)根据表中数据,推测出该有机物是由
提示:浓硫酸可以吸收水蒸气,氢氧化钠可以吸收二氧化碳.
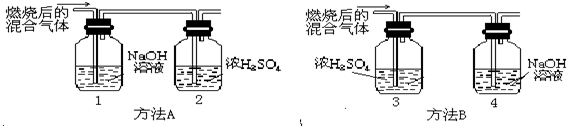
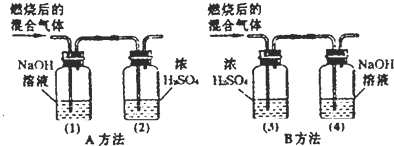 (2005?青浦区)某有机物在氧气中充分燃烧后,产物只有二氧化碳和水.甲、乙两组同学分别用A、两种方法(为如图所示)测定它的组成,得到两组数据(见下表).请你分析:浓H2SO4具有
(2005?青浦区)某有机物在氧气中充分燃烧后,产物只有二氧化碳和水.甲、乙两组同学分别用A、两种方法(为如图所示)测定它的组成,得到两组数据(见下表).请你分析:浓H2SO4具有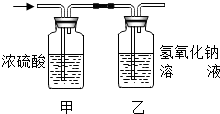 (2012?牡丹江)某有机物在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下:
(2012?牡丹江)某有机物在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下: